
初三化学(人教版)《原子结构(第二课时)》优质课件、教学设计、任务单、练习题
















教学目标:
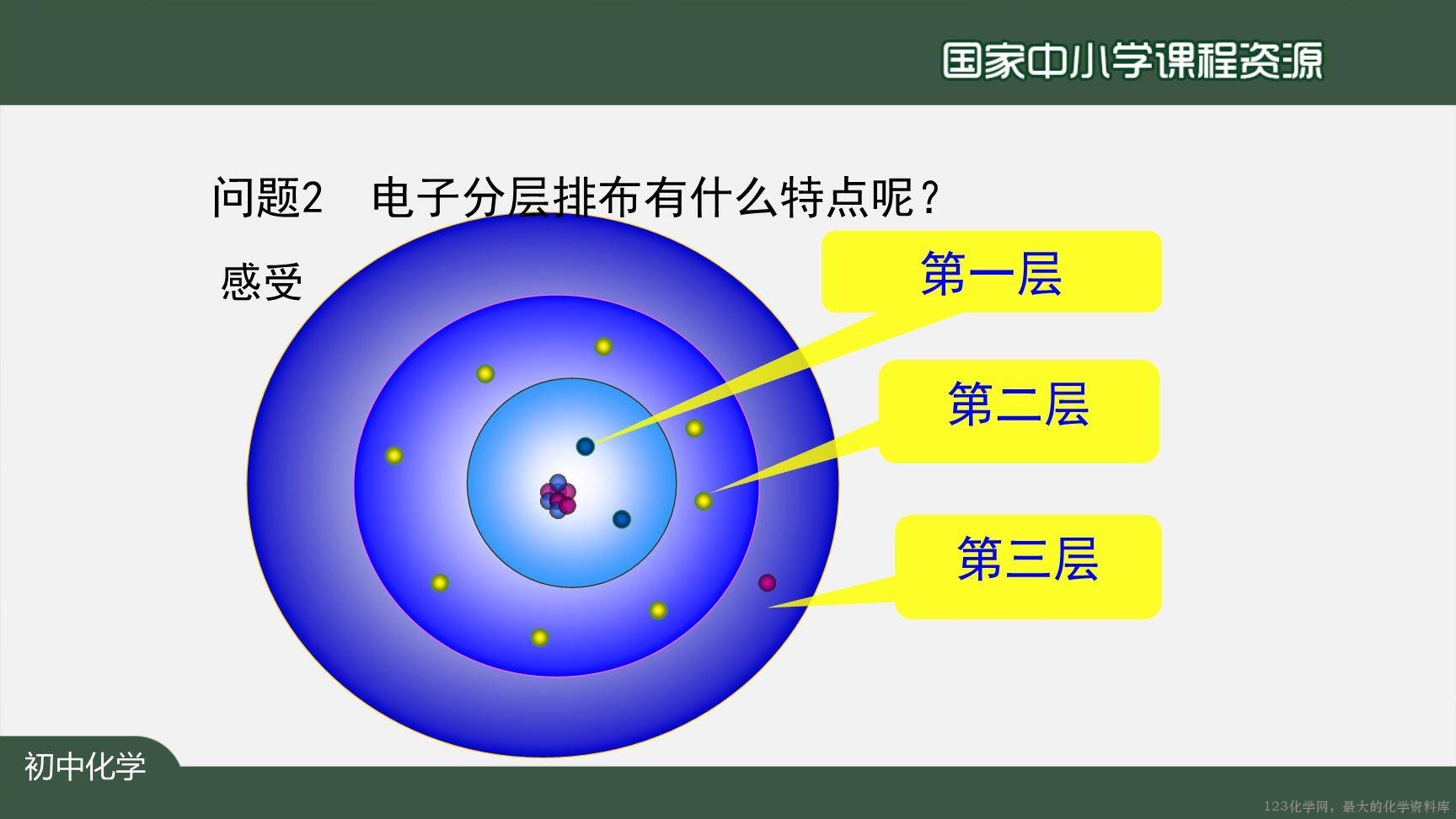
1.了解核外电子是分层排布的,了解典型原子(稀有气体、金属、非金属)原子核外电子的排布特点;
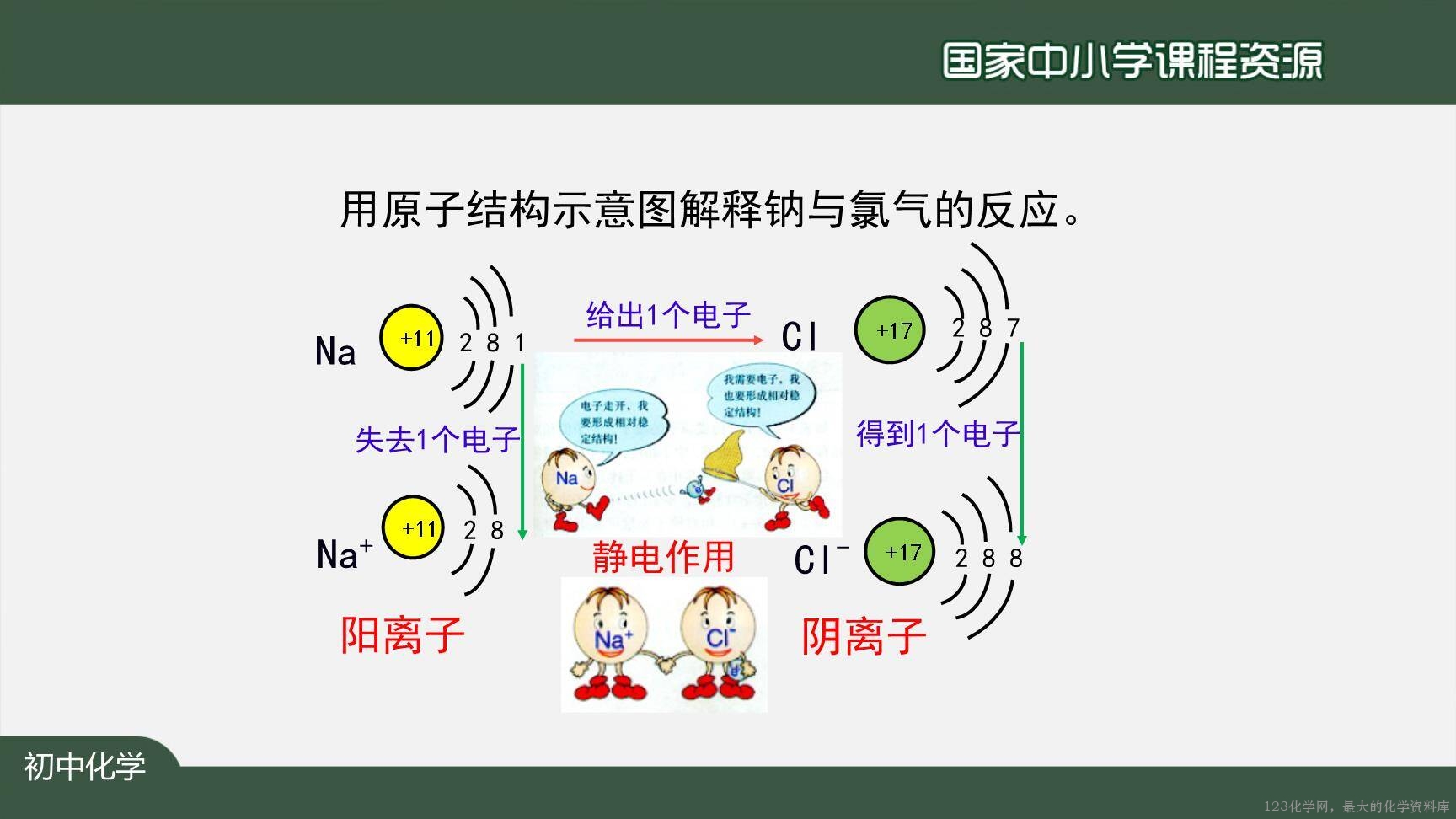
2.以氯化钠为例,了解离子的形成过程,知道离子是构成物质的一种粒子;
3.知道相对原子质量的含义。并学会查相对原子质量表。
教学重点:原子的核外电子分层排布;离子的形成;相对原子质量
教学难点:原子的核外电子排布;相对原子质量
主要师生活动
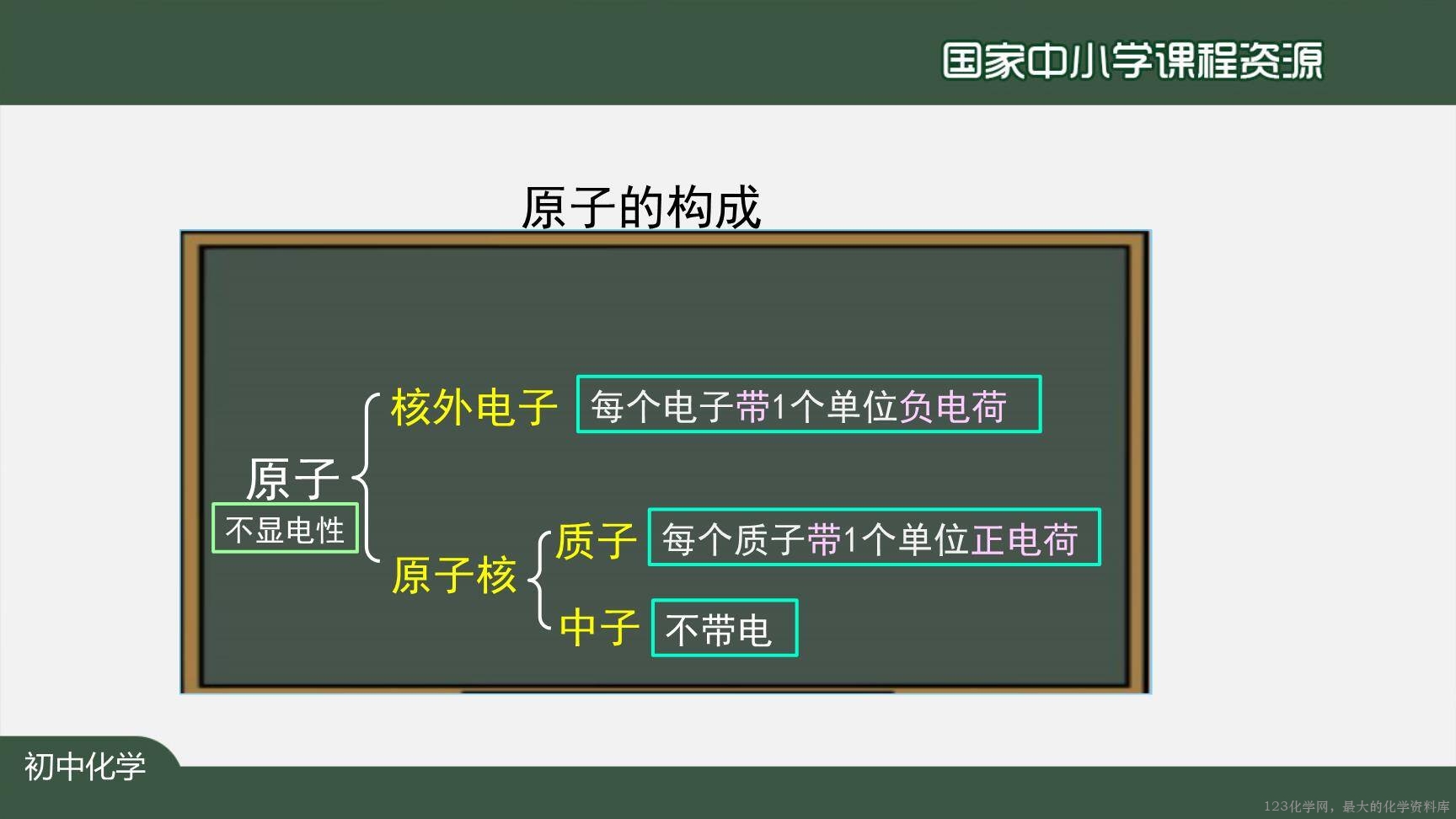
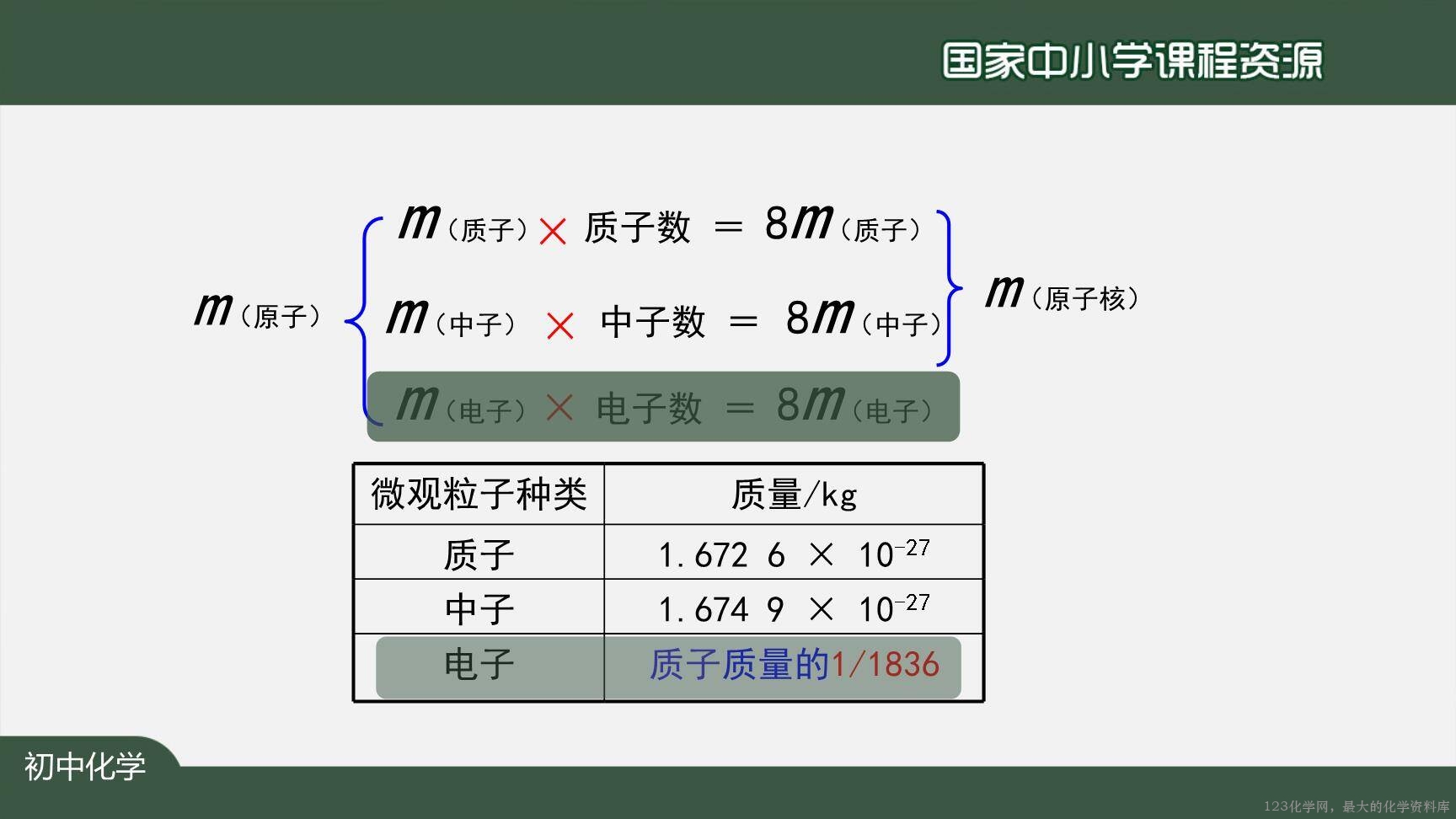
【复习】原子的构成、电性、粒子间的数量关系。
【讲解】介绍科学家们对原子核外电子的发现史,卢瑟福、波尔、薛定谔对核外电子的研究成果,提出了近代人类的研究结果,电子是分层运动的。
【学生活动1】画出核外电子运动图。
【讲解】核外电子的分层运动的特点。
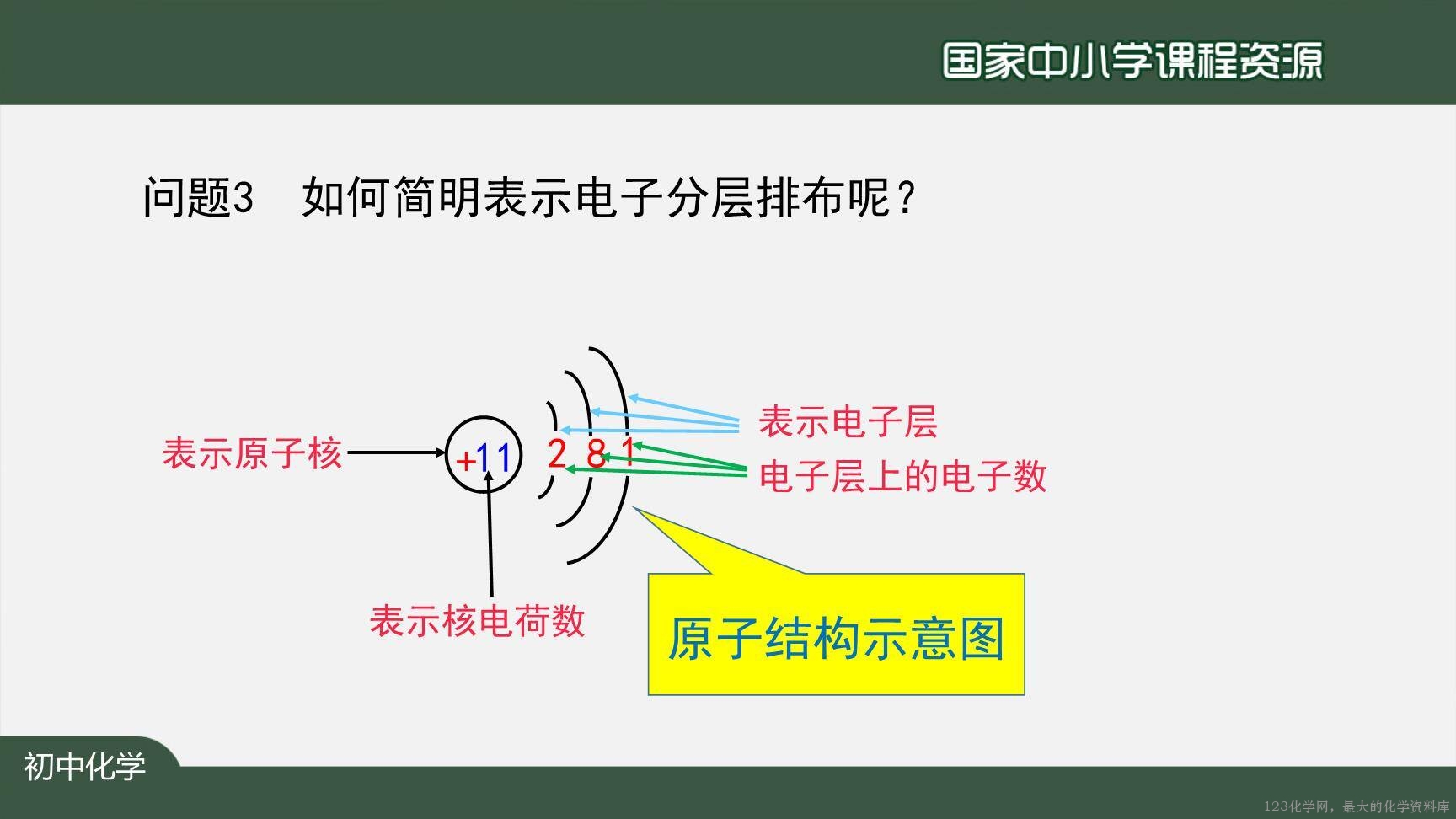
【学生活动2】根据事实,画出钠原子的结构示意图。
【讲解】原子结构示意图的画法。
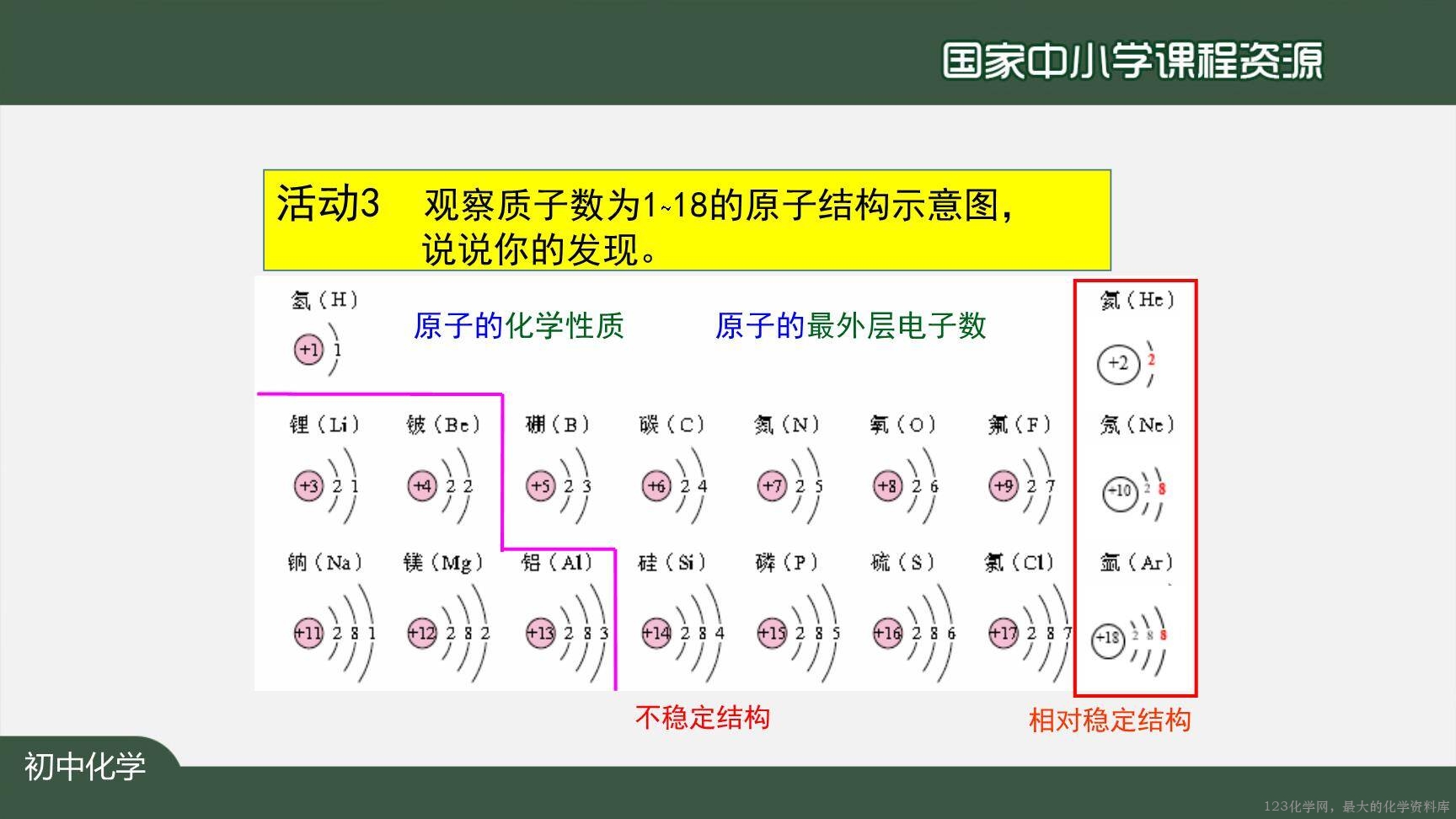
【学生活动3】参照质子数为1~18原子结构示意图,说说你的发现。
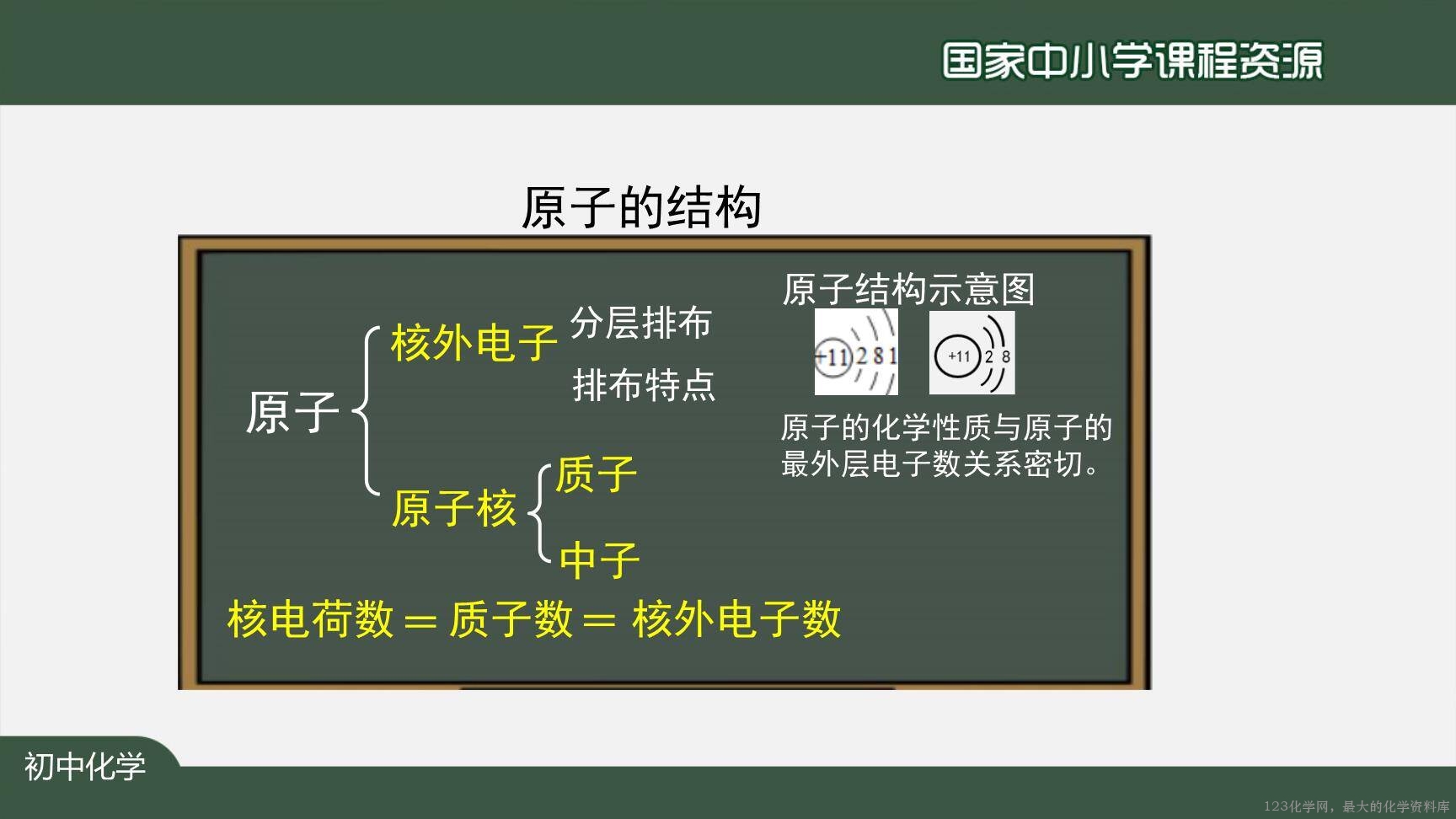
【讲解】根据学生的答案归纳原子核外电子排布特点,相对稳定结构,原子的化学性质与原子的最外层电子数的关系。
【指导】以氯化钠的形成过程为例,在学生思考的基础上,巩固对相对稳定结构的认识,体会到原子的化学性质与原子的最外层电子数的密切关系。
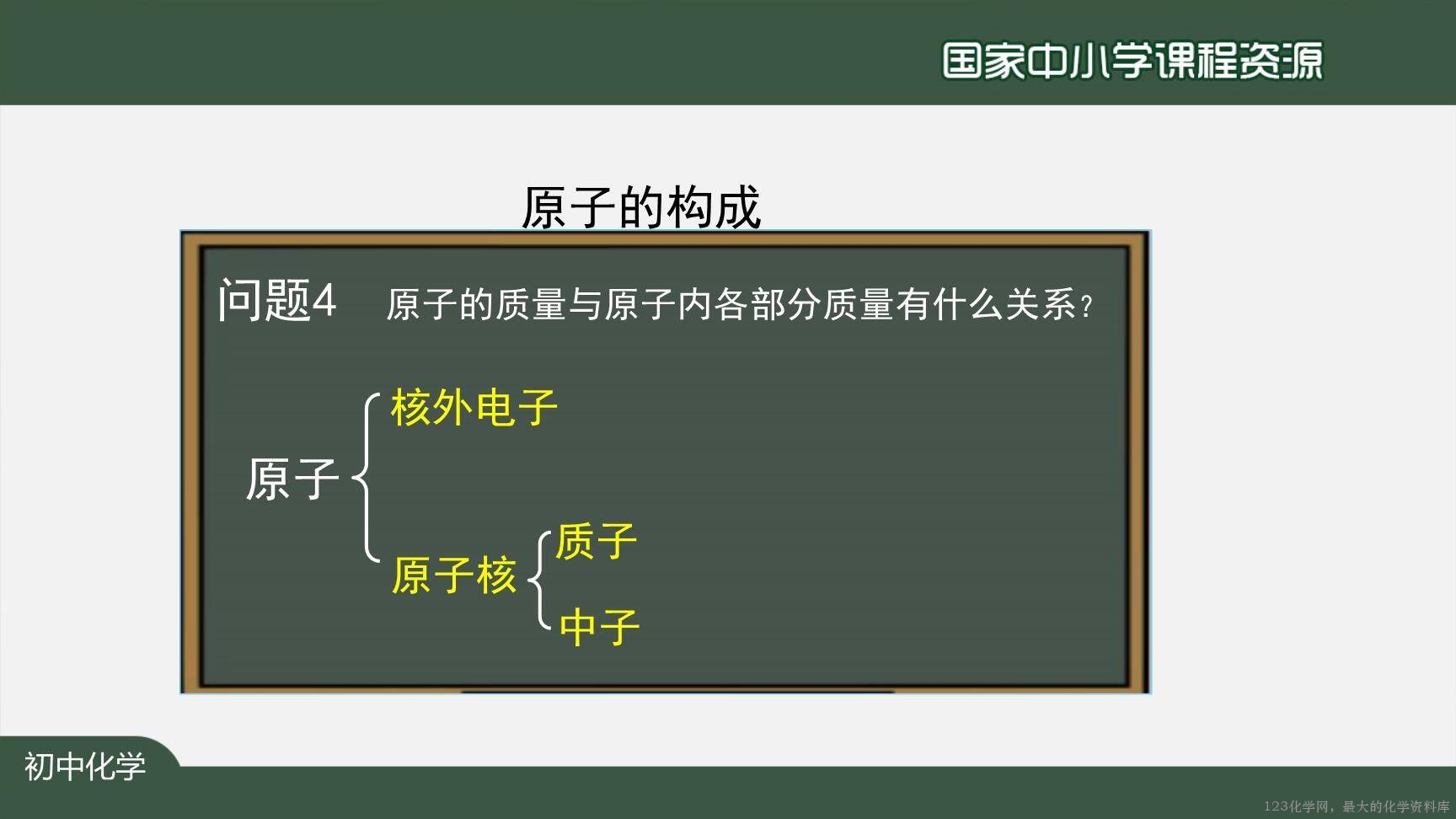
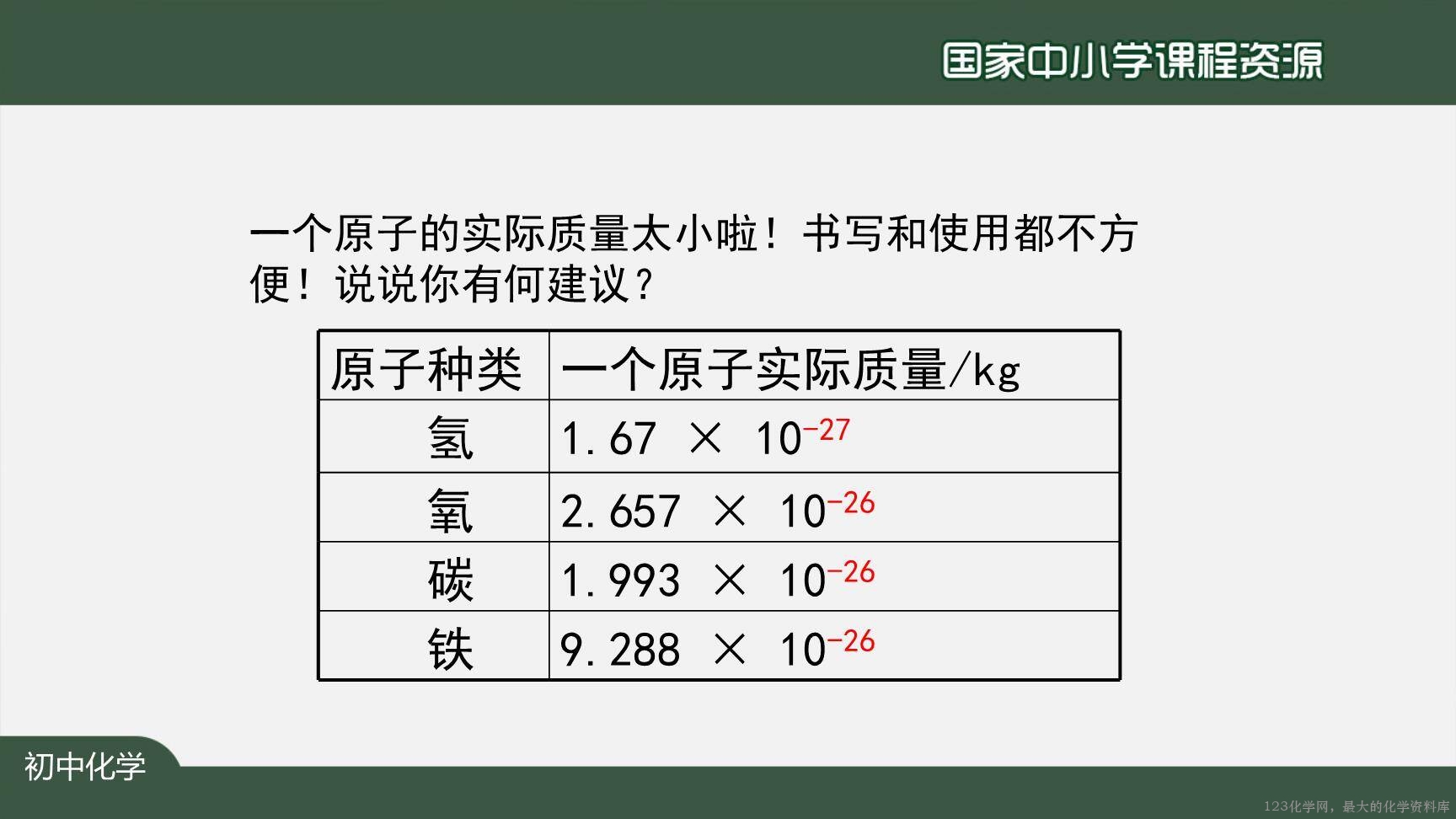
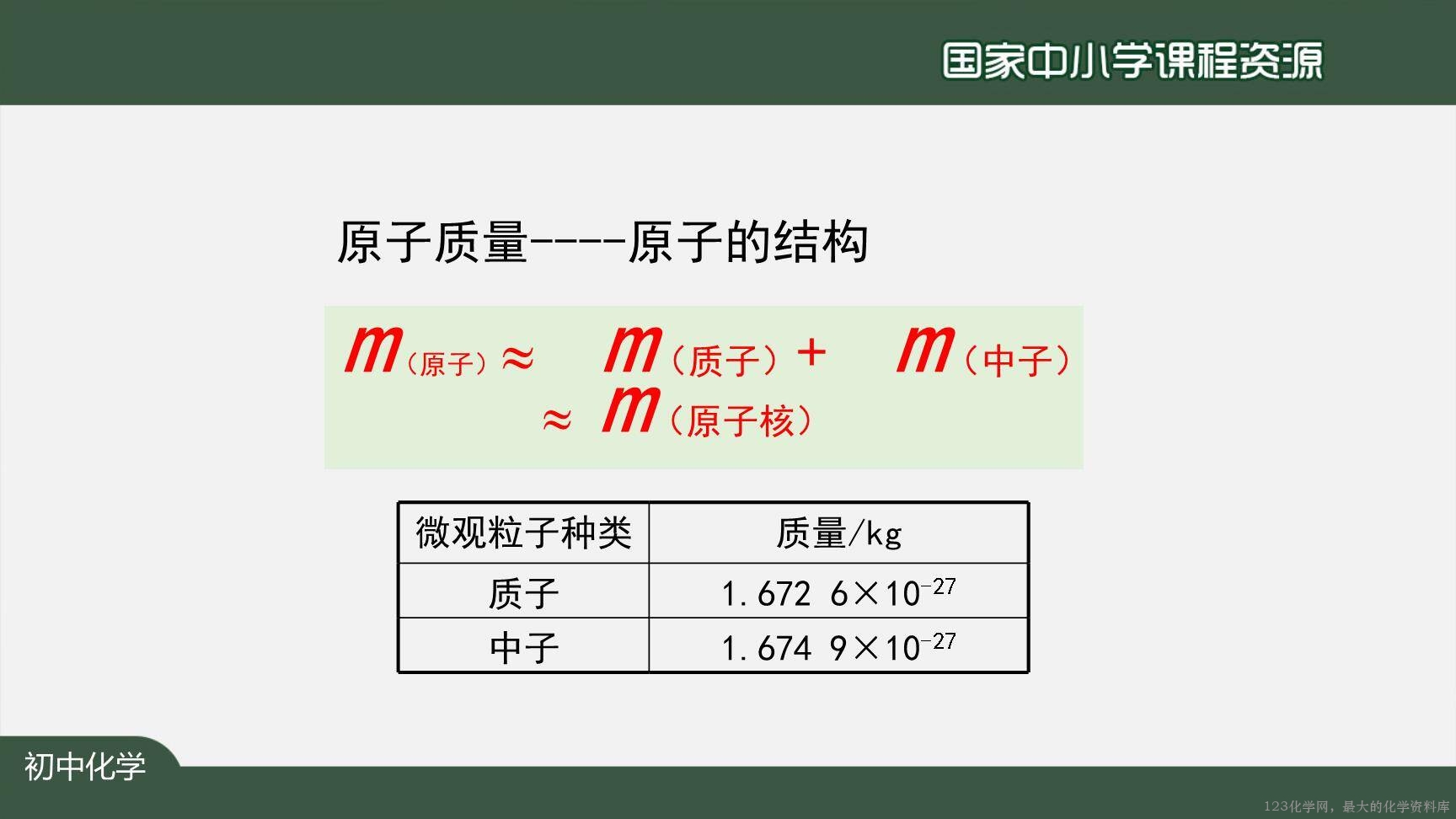
【感受】学生感知原子质量小,使用不方便, 思考如何科学化处理后方便交流和使用。
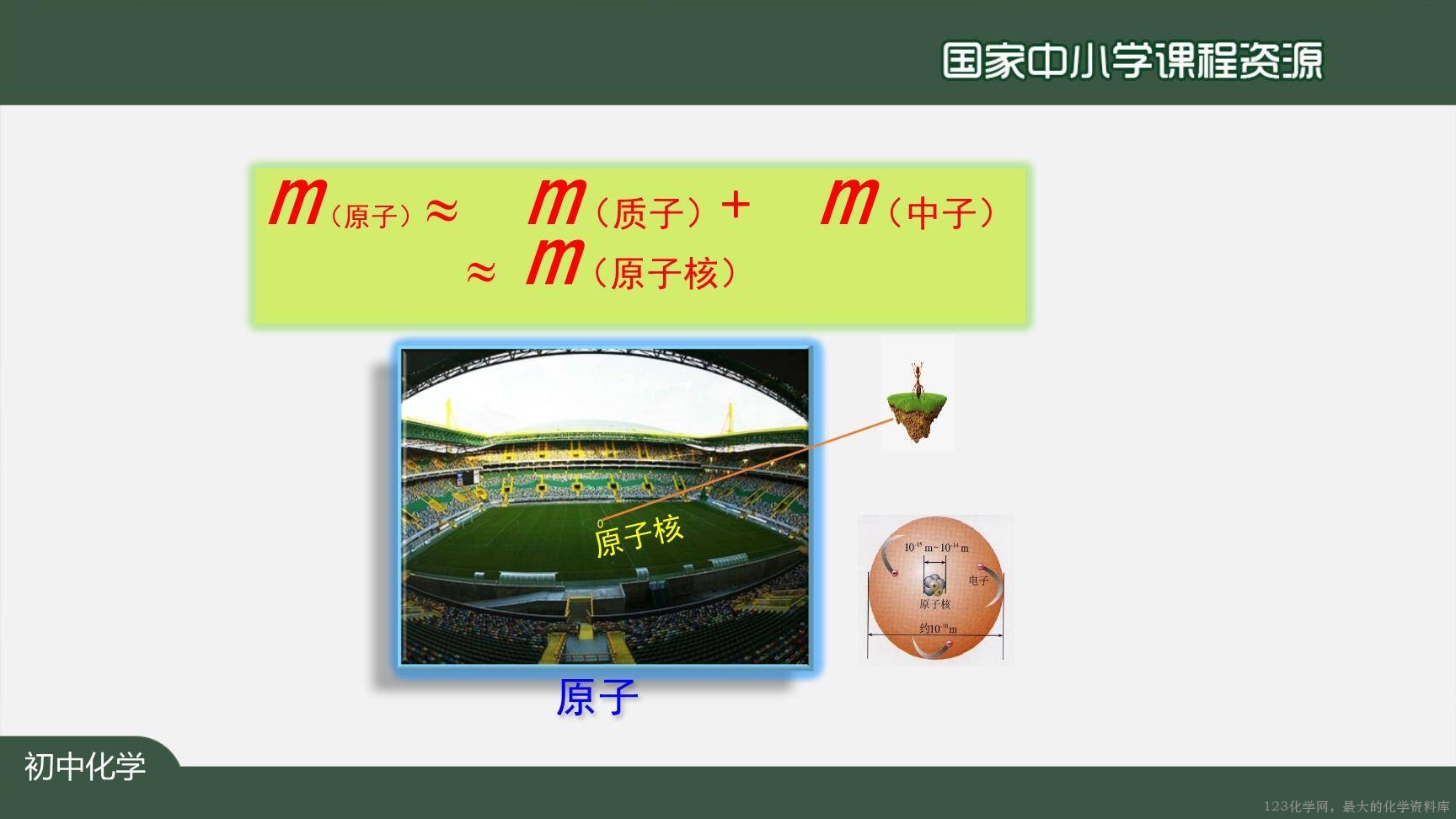
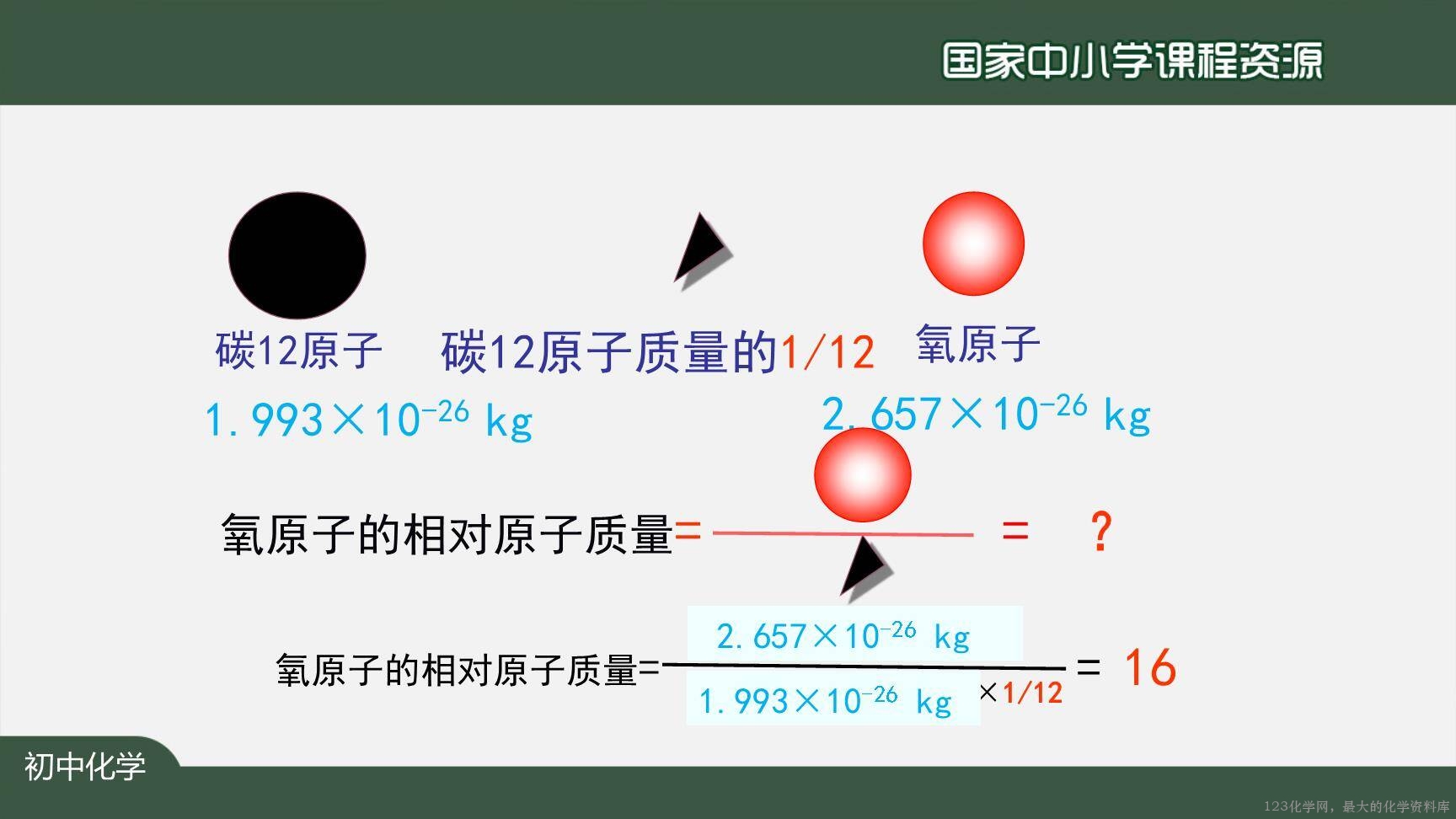
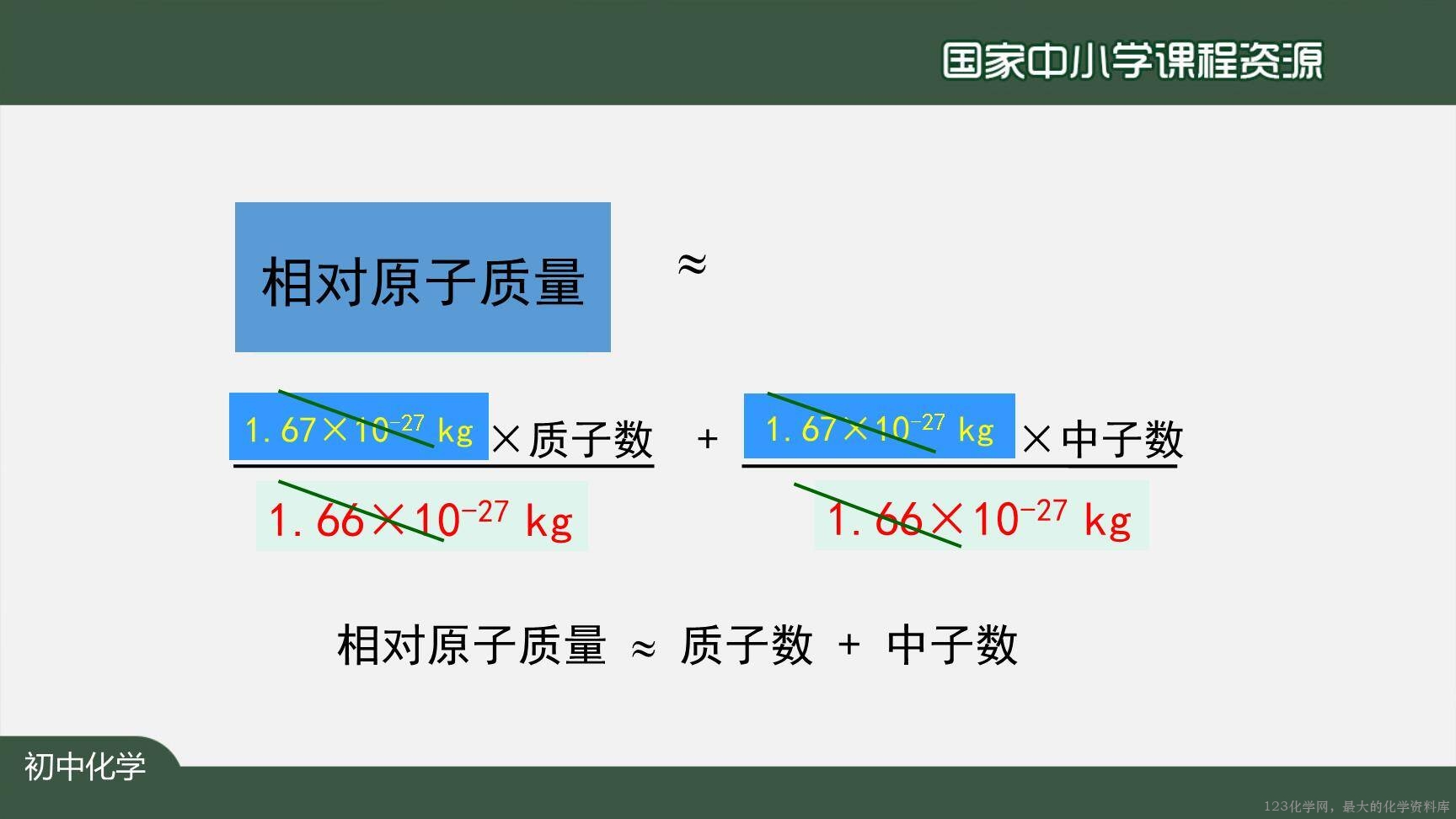
【讲解】相对原子质量的定义,相对原子质量与质子数中子数的关系。
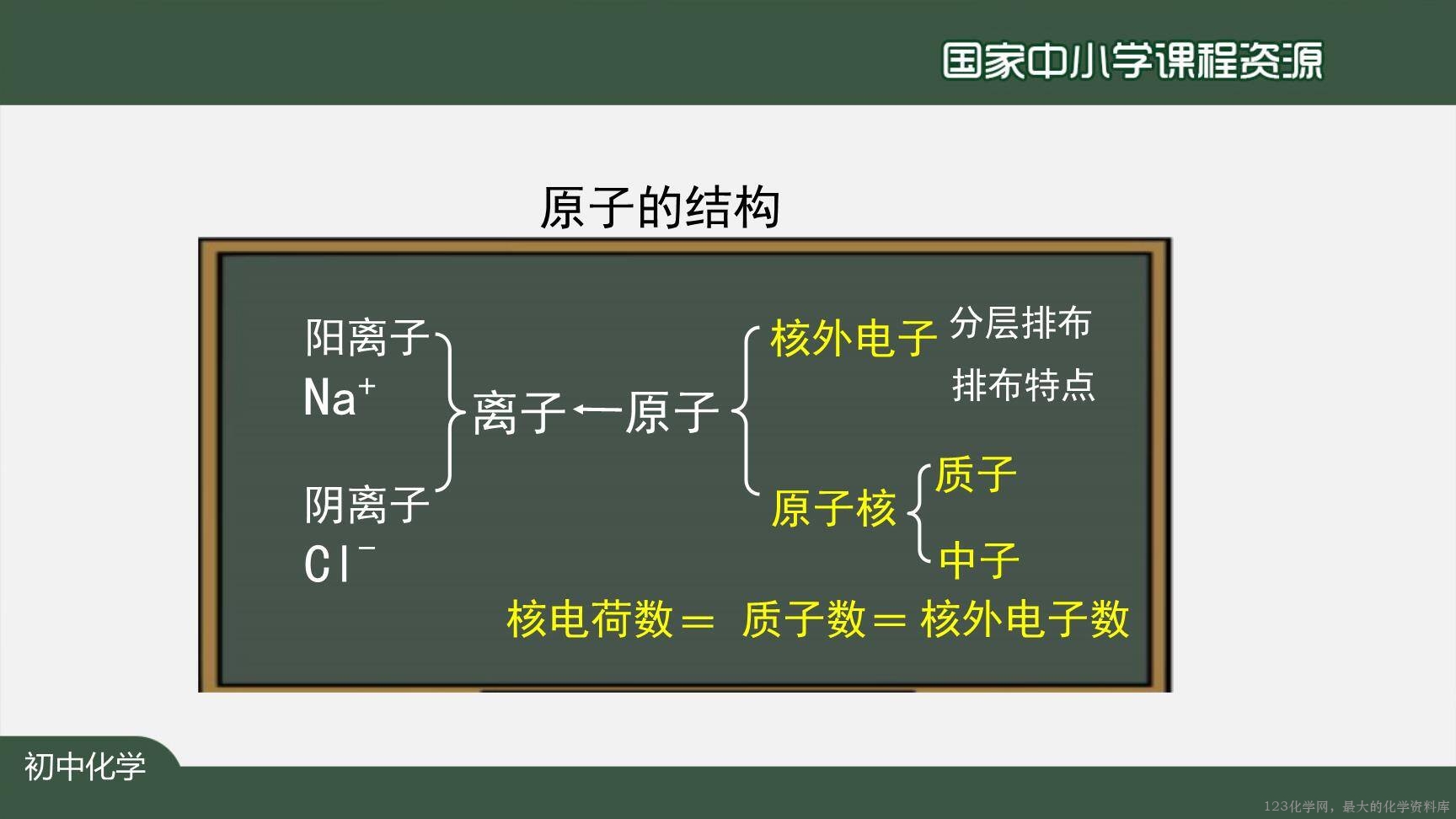
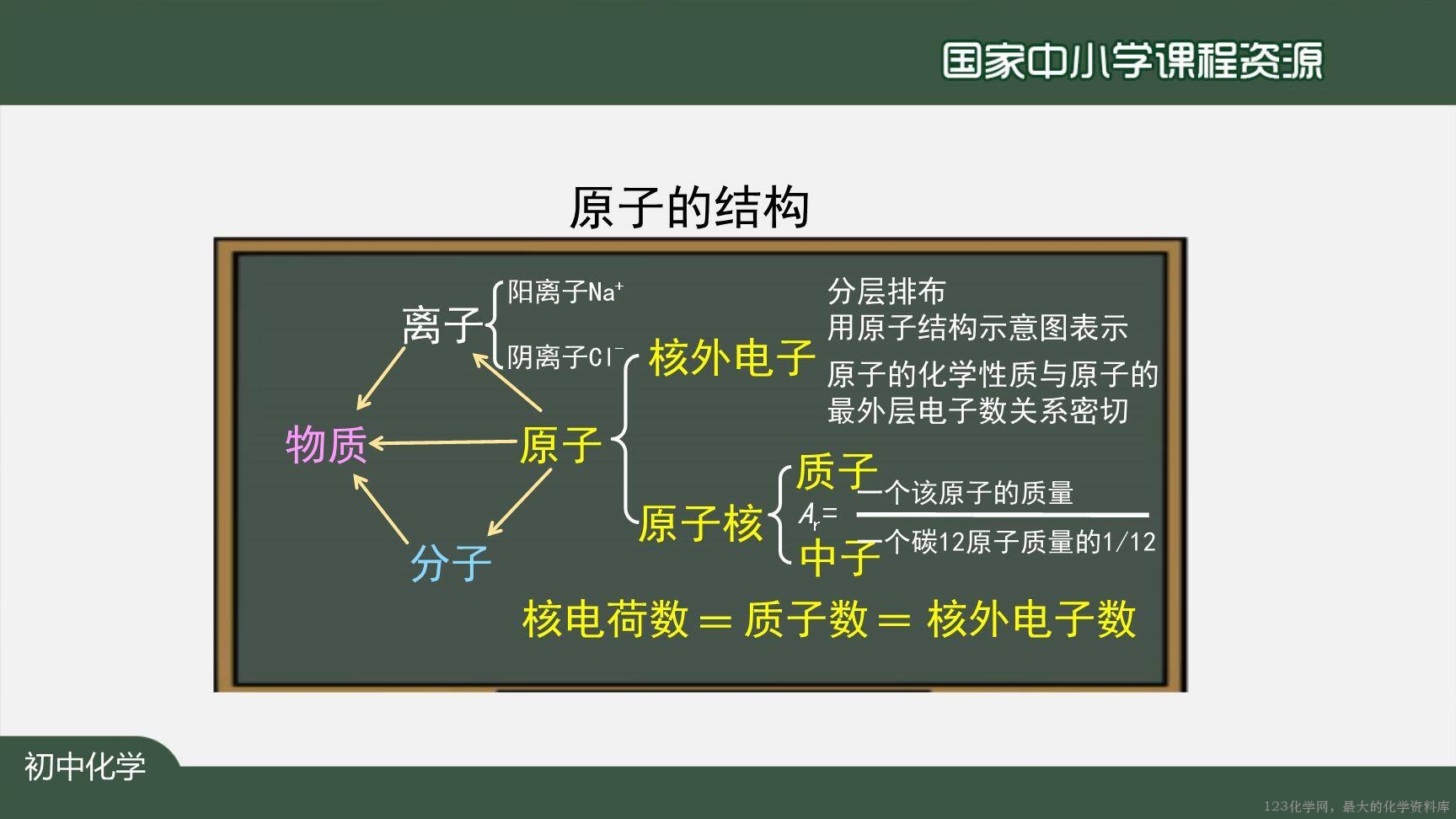
【总结】原子的结构。