2025高一化学新教材新理念新设计同步课堂人教版必修第二册6.2.2 化学反应的限度(基础过关原卷版)
2025高一化学新教材新理念新设计同步课堂人教版必修第二册6.2.2 化学反应的限度(基础过关原卷版)6.2.2化学反应的限度(练好题)解析版
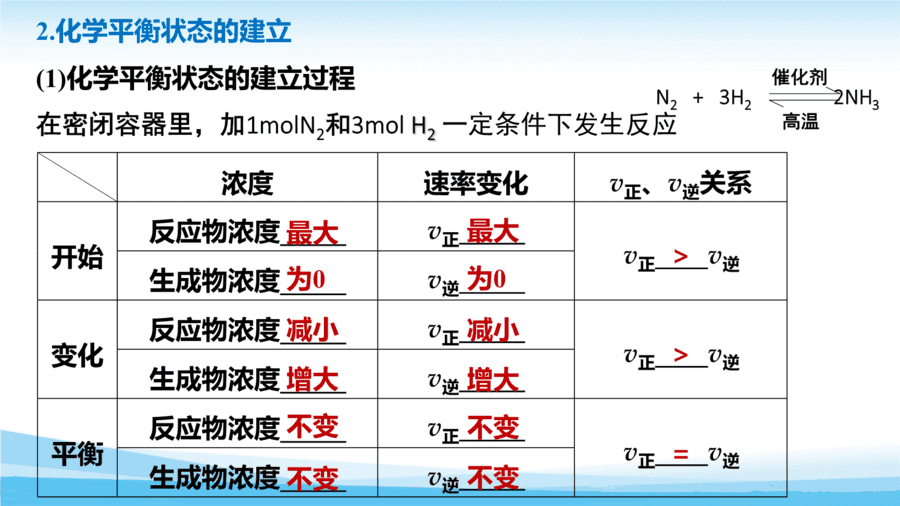
基础过关
1.下列反应不属于可逆反应的是( )
A.二氧化硫的催化氧化
B.氯气溶于水
C.工业合成氨
D.水电解生成H2和O2与H2在O2中的燃烧反应
【答案】 D
【解析】 二氧化硫的催化氧化生成SO3是可逆反应,故A正确;氯气溶于水,氯气与水反应生成HCl和HClO,是可逆反应,故B正确;工业合成氨是可逆反应,故C正确;水电解生成H2和O2与H2在O2中的燃烧反应,反应条件不同,不是可逆反应,故D错误。
2.下列关于化学平衡的说法中,正确的是 ( )
A.当达到化学平衡时,反应物已完全转化为生成物
B.化学平衡是一定条件下的平衡,当条件改变时,平衡可能会遭到破坏
C.当达到化学平衡时,反应混合物中各成分的浓度相等
D.当达到化学平衡时,正逆反应均已停止
【答案】 B
【解析】 当可逆反应达到化学平衡时,正、逆反应速率相等,但并未停止,此时反应体系中各成分的浓度不再改变(但不一定相等),当外界条件发生改变时,平衡可能被破坏,B正确,C、D错误;可逆反应中,反应物的转化率达不到100%,A错误。
3.500 ℃时,将2 mol N2和2.25 mol H2充入体积为10 L的恒容密闭容器中,反应达到平衡时,NH3的浓度不可能是( )
A.0.1 mol·L-1 B.0.12 mol·L-1
C.0.05 mol·L-1 D.0.16 mol·L-1
【答案】 D
【解析】 由题干信息可知,N2和H2发生反应生成NH3,反应方程式为N2+3H2高温、高压催化剂2NH3,该反应中N2过量,假设2.25 mol H2完全反应,则生成NH3的物质的量为1.5 mol,浓度为
0.15 mol·L-1,但该反应是可逆反应,H2不可能完全转化为NH3,因此达到平衡时,NH3的浓度小于0.15 mol·L-1,D选项符合题意。