
2025~2026高中化学选择性必修1教案学案22第四章第二节第2课时电解原理的应用










电解总反应
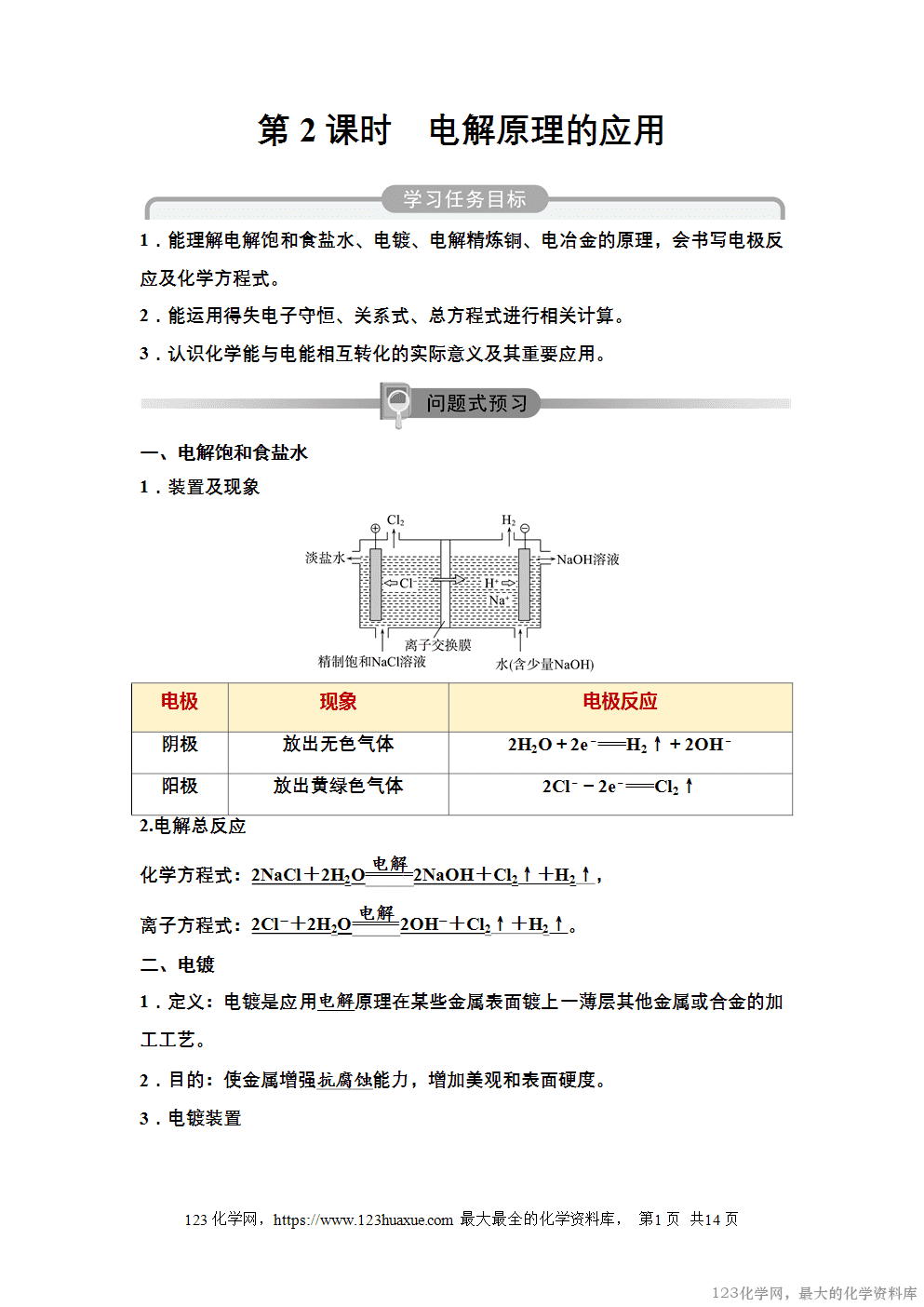
化学方程式:2NaCl+2H2O2NaOH+Cl2↑+H2↑,
离子方程式:2Cl-+2H2O2OH-+Cl2↑+H2↑。
二、电镀
1.定义:电镀是应用电解原理在某些金属表面镀上一薄层其他金属或合金的加工工艺。
2.目的:使金属增强抗腐蚀能力,增加美观和表面硬度。
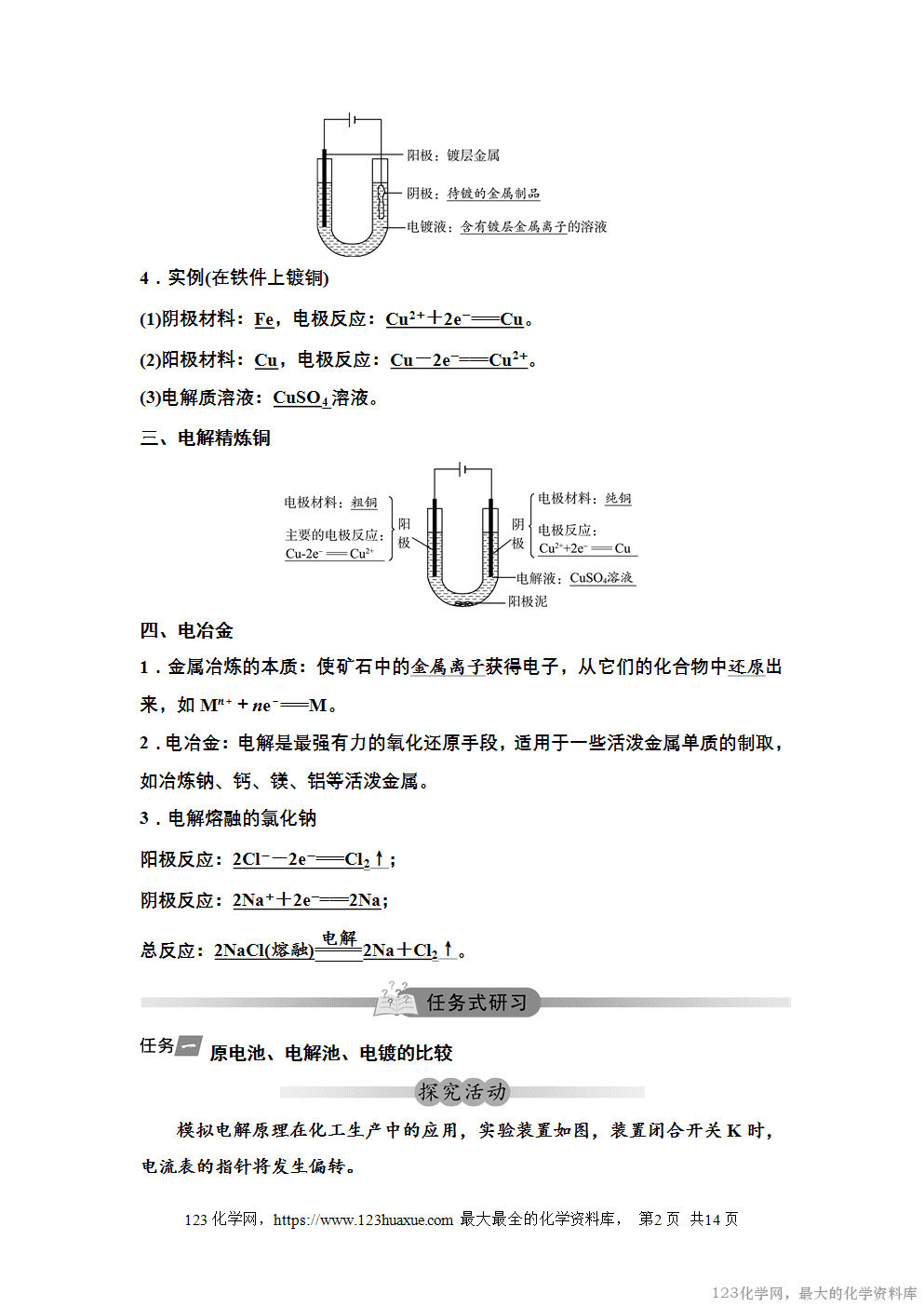
3.电镀装置
4.实例(在铁件上镀铜)
(1)阴极材料:Fe,电极反应:Cu2++2e-===Cu。
(2)阳极材料:Cu,电极反应:Cu-2e-===Cu2+。
(3)电解质溶液:CuSO4溶液。
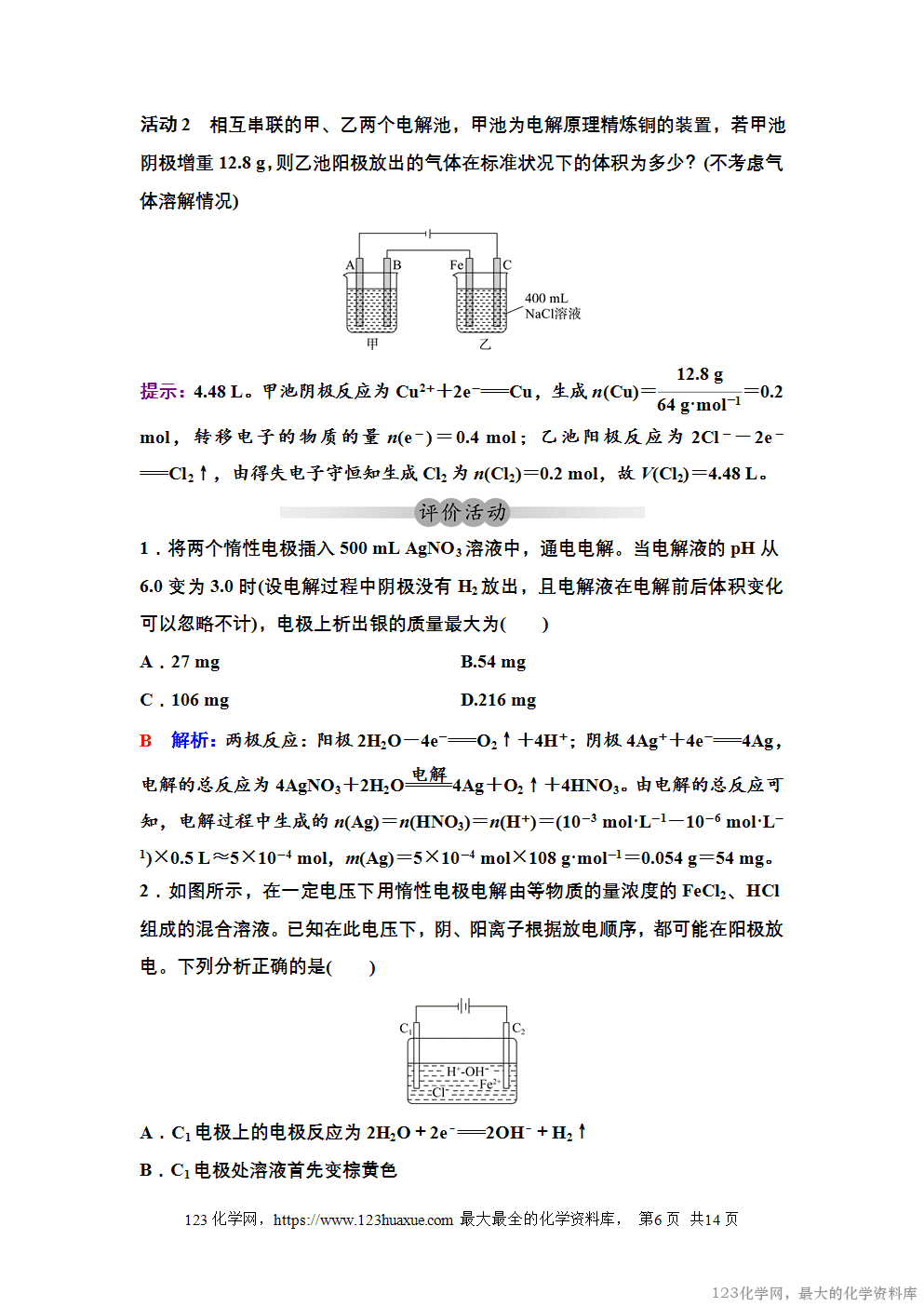
三、电解精炼铜
四、电冶金
1.金属冶炼的本质:使矿石中的金属离子获得电子,从它们的化合物中还原出来,如Mn++ne-===M。
2.电冶金:电解是最强有力的氧化还原手段,适用于一些活泼金属单质的制取,如冶炼钠、钙、镁、铝等活泼金属。
3.电解熔融的氯化钠
阳极反应:2Cl--2e-===Cl2↑;
阴极反应:2Na++2e-===2Na;
总反应:2NaCl(熔融)2Na+Cl2↑。
原电池、电解池、电镀的比较
模拟电解原理在化工生产中的应用,实验装置如图,装置闭合开关K时,电流表的指针将发生偏转。