

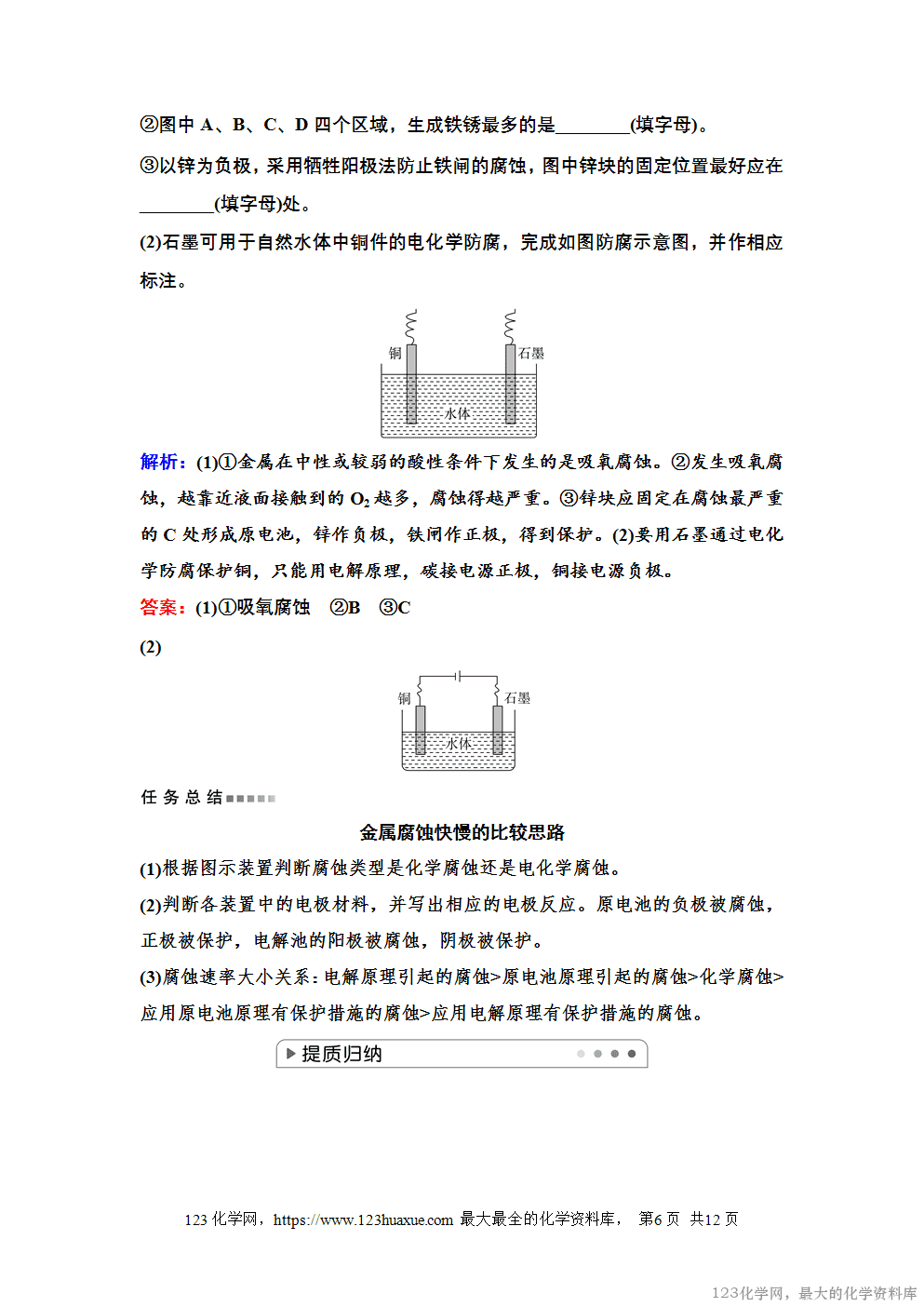



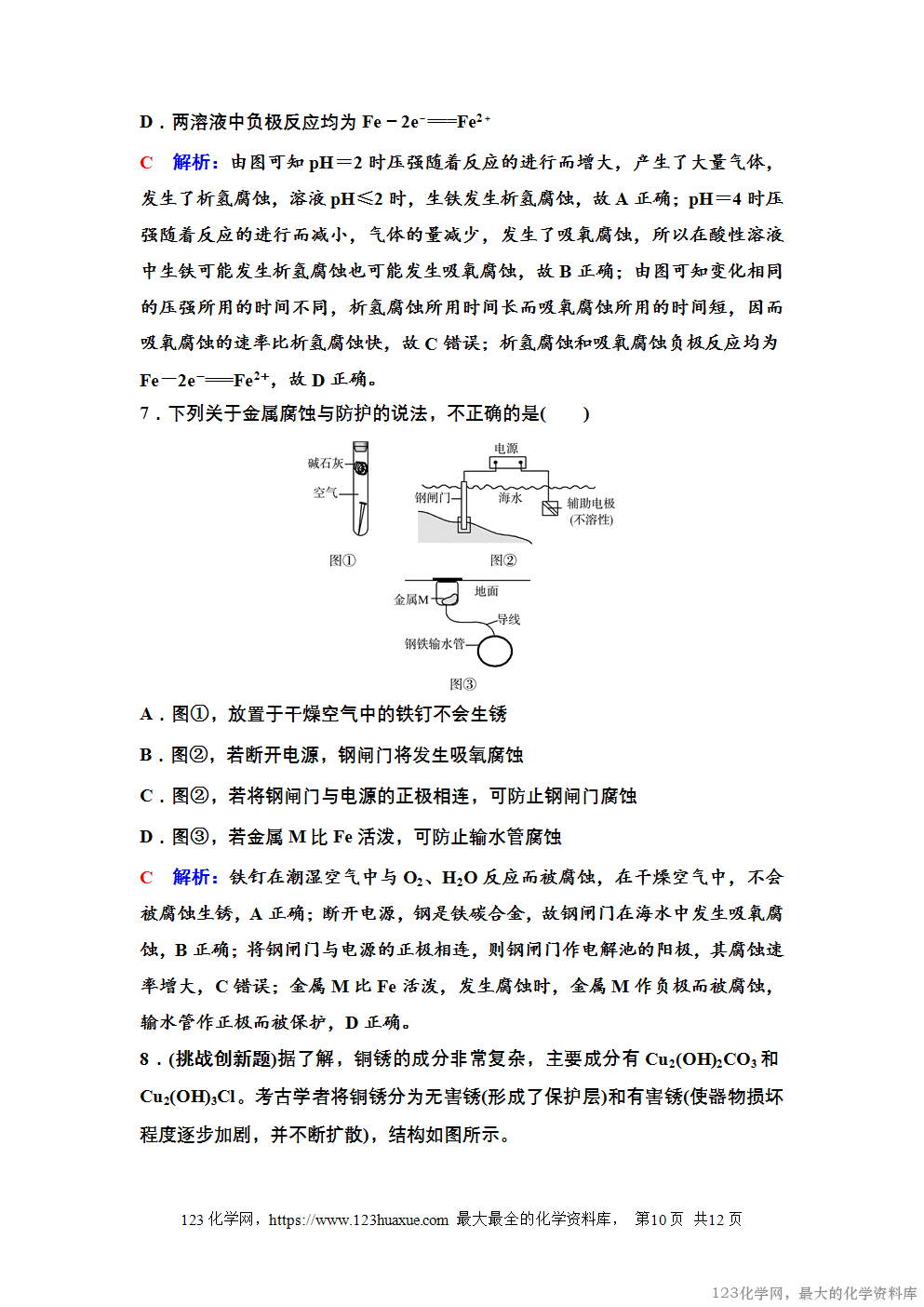

实验探究金属的腐蚀
(1)将经过酸洗除锈的铁钉和饱和食盐水浸泡一下,放入具支试管中,几分钟后,可以观察到的现象是导管中的液面上升,说明铁发生了吸氧腐蚀。
(2)取两支试管,分别放入两颗锌粒和等体积、等浓度的稀硫酸,实验现象是两支试管中均有气泡产生,反应的离子方程式为Zn+2H+===Zn2++H2↑,向其中一支试管中滴加1~2滴硫酸铜溶液,观察到的现象是产生气泡速率增大,原因是锌置换出铜,形成原电池。
二、金属的防护
1.金属的防护方法
2.金属的电化学防护
(1)牺牲阳极法
①理论依据:利用原电池原理。
②装置示意图
③电极反应
负极:Zn-2e-===Zn2+;
正极:2H++2e-===H2↑。
(2)外加电流法
①理论依据:利用电解原理。
②装置示意图
金属的腐蚀与防护
港珠澳大桥在世界桥梁建筑历史上创造了无数奇迹,里程最长,施工难度最大,设计使用寿命最长,技术含量最高……在大桥应用的多项关键技术中,由中国科学院金属研究所提供的桥基钢管复合桩系列防腐解决方案,为保证大桥达到120年的超长寿命发挥了关键作用。
活动1 地下钢管生锈属于哪种类型的电化学腐蚀?
提示:属于吸氧腐蚀。
活动2 写出钢管生锈时两极的电极反应。
提示:Fe作负极,电极反应为2Fe-4e-===2Fe2+;C作正极,电极反应为O2+2H2O+4e-===4OH-。
活动3 为保护地下钢管不被腐蚀,可采取的电化学防护措施有哪些?
提示:将钢管与锌板相连,或将钢管与直流电源负极相连。
1.为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化的3% NaCl溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )