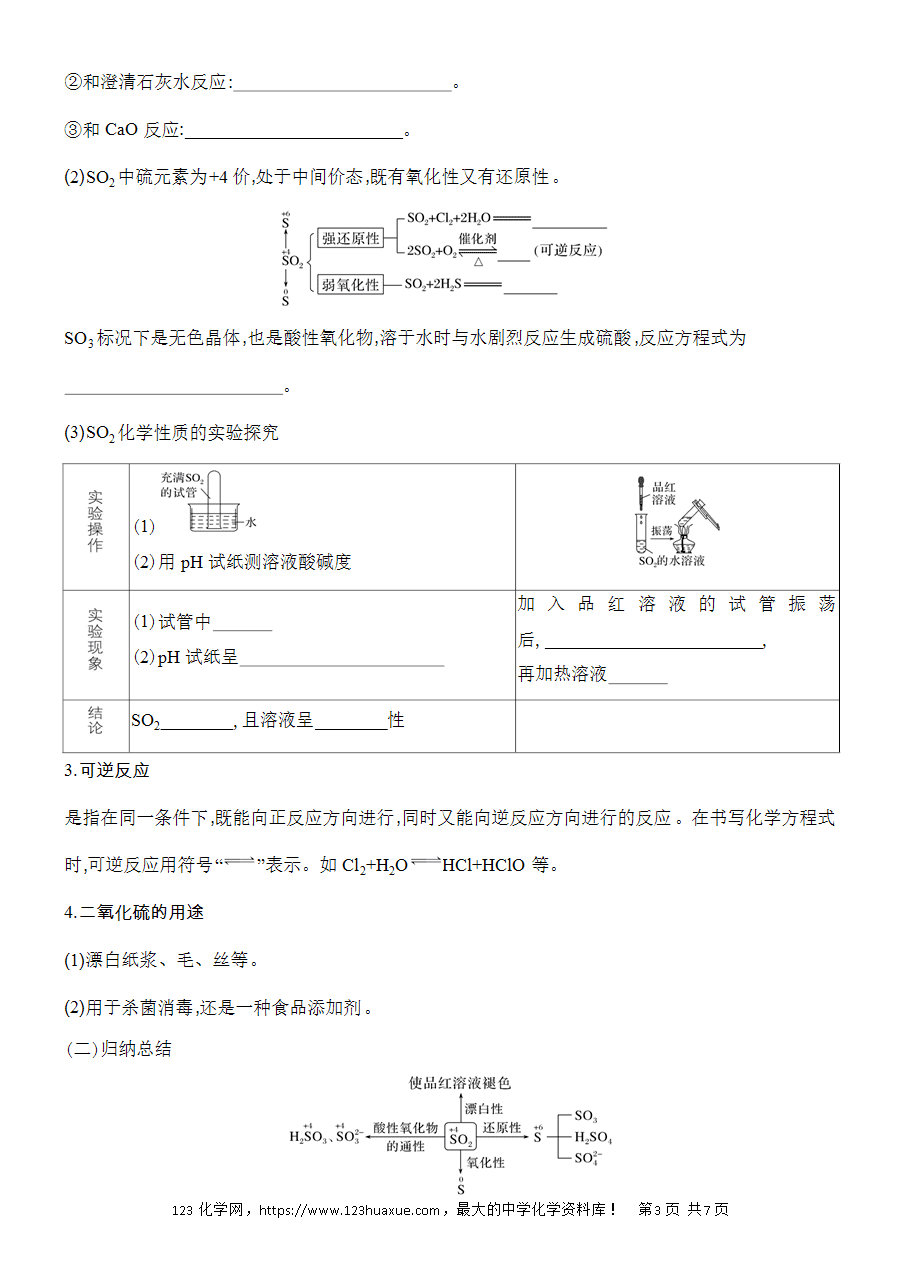
归纳总结
1.硫以游离态和化合态形式存在。硫有多种同素异形体,如正交硫和斜方硫。
2.从物质类别和元素化合价角度理解硫的化学性质:
H2O2、
3.硫在一定条件下与大多数金属反应生成相应的金属硫化物,与变价金属反应生成其低价金属硫化物。
4.硫与氧气反应,不论氧气是否足量、浓度如何,其一步反应都只能生成SO2,不能生成SO3。
5.硫可与热的NaOH溶液反应3S+6NaOH2Na2S+Na2SO3+3H2O(可以清洗试管壁残留的硫)。硫与汞常温下反应:Hg+S===HgS, 可以用来去除洒落的汞。
1.关于单质硫的叙述有:①通常状况下为黄色粉末;②不溶于水、微溶于酒精、易溶于二硫化碳;③氧化性比氯气弱;④只能被还原不能被氧化;⑤医药上用来做硫黄软膏治疗某些皮肤病。其中正确的是 ( )
A.①②③⑤ B.②③⑤
C.②④⑤ D.③⑤
2.下列化合物中,不能由组成该化合物的两种元素的单质直接化合而成的是