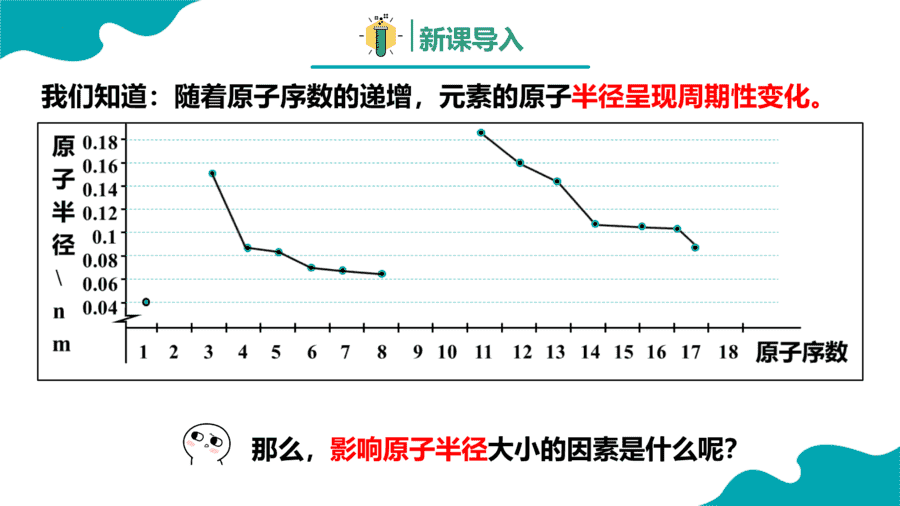
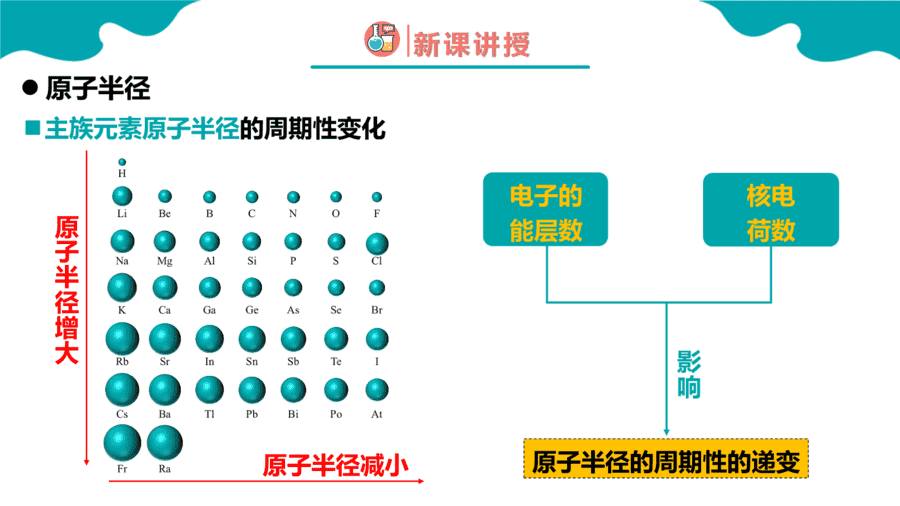
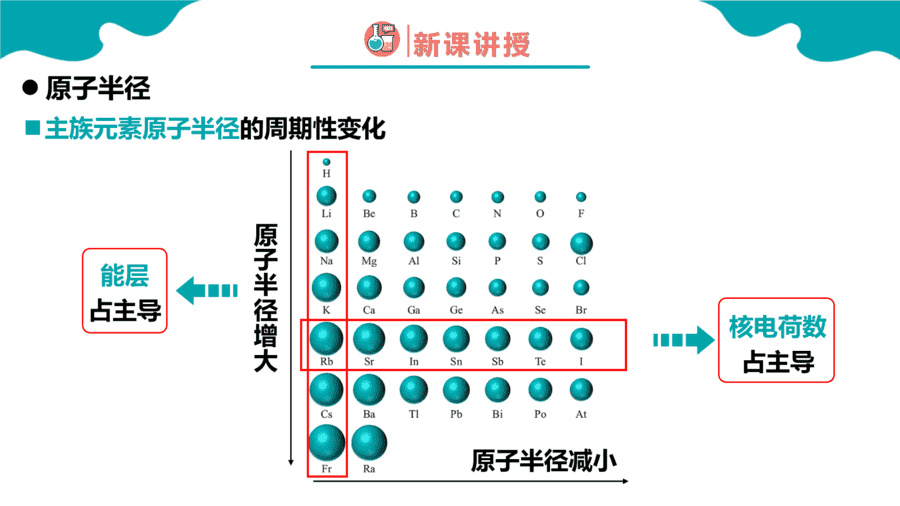
1. Na、Mg、Al均为第三周期元素。下列说法正确的是
A.离子半径:
B.第一电离能:
C.还原性:
D.碱性:
【答案】C
【详解】A.三种离子核外电子排布相同半径随核电荷数增大而减小,故A错误;
B.同周期元素第一电离能总体趋势:核电荷数越大,第一电离能越大,故B错误;
C.同周期元素,核电荷数越大金属性越弱,对应单质还原性越弱,故C正确;
D.金属性,其对应最高价氧化物水化物碱性越弱,碱性:,故D错误;
故选C。
2.(2022下·云南保山·高二统考期末)形成简单离子的最外层电子排布均为,且半径依次减小。C、D、E原子中均仅有一个未成对电子。单质为双原子分子,化学性质稳定。组成典型的离子化合物,其晶体结构类似于晶体。下列说法正确的是
A.简单气态氢化物的稳定性:
B.简单离子的氧化性:
C.第一电离能:
D.单质与的最高价氧化物对应的水化物均可发生反应
【答案】D
【详解】形成简单离子的最外层电子排布均为,且半径依次减小。C、D、E原子中均仅有一个未成对电子。单质为双原子分子,化学性质稳定,A为氮。组成典型的离子化合物,其晶体结构类似于晶体,C为氟、D为钠。B为氧,E为铝。
A.简单气态氢化物的稳定性应为HF>H2O>NH3,A错误;
B.简单离子的氧化性:Al3+>Na+,B错误;
C.第一电离能:F>N>O,C错误;
D.铝能和硝酸或氢氧化钠反应,D正确;
故选D。