
关于如图所示的原电池甲和乙,下列说法正确的是
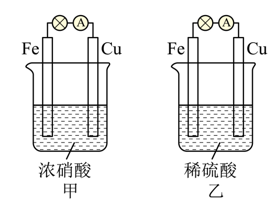
A.甲、乙中铜片上均发生还原反应 B.两池中铁片均发生反应:Fe-2e-=Fe2+
C.装置甲中电子由Cu→灯泡→Fe D.两池所得Fe、Cu金属活泼性相反
【答案】C
【详解】A.甲池中在室温下Fe在浓硝酸中会钝化,Cu与硝酸会发生剧烈反应,所以Cu作负极,失去电子发生氧化反应;在乙池中由于Fe比Cu活泼,Fe与稀硫酸发生反应,所以铁作负极,失去电子发生氧化反应,Cu做正极,正极上发生H+得到电子的还原反应,A错误;
B.甲池中铜作负极,电极反应为Cu-2e-=Cu2+,乙池中Fe为负极,发生电极反应:Fe-2e-=Fe2+,B错误;
C.甲池中铜作负极、铁作正极,电子由负极(Cu)经过用电器(灯泡)到达正极(Fe),C正确;
D.在原电池中一般活泼金属作负极,不活泼的作正极,但根据电极反应判断金属活泼性时,还要结合电解质溶液的酸碱性及电解质浓度对电极判断的影响,D错误;
故合理选项是C。
资料标签: