空间构型为正八面体。
同一原子内由1个s轨道、3个p轨道和2个d轨道参与的杂化称为sp3d2杂化,所形成的6个杂化轨道称sp3d2杂化轨道。各含有1/6的s成分、1/2的p成分和1/3的d成分,杂化轨道间的夹角为90°,空间构型为正八面体。
sp杂化
进行sp杂化时,每个杂化轨道由1/2(ns)轨道和1/2(np)轨道组合而成,两个杂化轨道之间的夹角为180°。因此由sp杂化轨道构成的分子具有直线形的构型。
sp2杂化
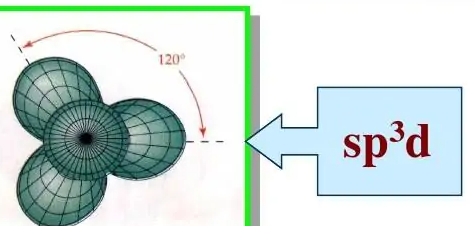
同一个原子内的ns轨道与两个np轨道杂化,形成三个等同的sp2杂化轨道,并分别与自旋相反的电子结合,形成三个σ键,其相互间夹角为120°。因此经sp2杂化而形成的分子具有平面三角形的构型。
sp3杂化
2s轨道与2p轨道实行sp3杂化后,已经成对的两个电子占据一个杂化轨道,三个未成对电子则各占一个杂化轨道,再按电子配对法共与三个电子自旋相反的氢原子形成三个共价键,因此分子呈三角锥构型。