
第1课时 化学平衡状态
1.一定条件下,对于可逆反应X(g)+3Y(g)2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是( D )
A.c1︰c2=3︰1
B.平衡时,生成Y和Z的速率之比为2︰3
C.X、Y的转化率不相等
D.c1的取值范围为0<c1<0.14 mol·L-1
解析:X、Y两种物质平衡时的浓度之比为1︰3,转化浓度之比也为1︰3,故c1︰c2=1︰3,A、C不正确;生成Y表示逆反应速率,生成Z表示正反应速率,平衡时v生成(Y)︰v生成(Z)应为3︰2,B不正确;由“极端假设法”可知0<c1<0.14 mol·L-1。
2.已知:K3[Fe(CN)6]溶液是检验Fe2+的试剂,若溶液中存在Fe2+,将产生蓝色沉淀。将0.2 mol·L-1的KI溶液和0.05 mol·L-1的Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明下列溶液中存在化学平衡“2Fe3++2I-2Fe2++I2”的是( A )
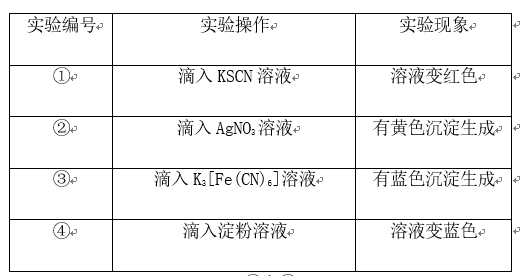
资料标签: