
第1课时 原电池的工作原理
1.锌铜原电池装置如图所示,下列说法正确的是( B )
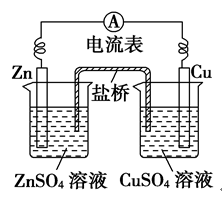
A.铜片作负极
B.锌电极的反应式:Zn-2e-===Zn2+
C.电流从锌片流向铜片
D.盐桥的作用是传递电子
解析:A项,Zn易失电子发生氧化反应而作负极,错误;B项,Zn易失电子发生氧化反应,锌电极的反应式:Zn-2e-===Zn2+,正确;C项,铜作正极,电流由铜片流向锌片,错误;D项,盐桥的作用是传递离子,电子不能通过溶液,错误。
2.有A、B、C、D四种金属。将A与B用导线连接起来,浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸中,D比A反应剧烈。将铜浸入B的盐溶液里,无明显变化。如果把铜浸入C的盐溶液里,有金属C析出。据此判断它们的活动性由强到弱的顺序是 ( B )
A.D>C>A>B B.D>A>B>C
C.D>B>A>C D.B>A>D>C
解析:将A与B用导线连接起来,浸入电解质溶液中,该装置构成了原电池,原电池中较活泼的金属作负极,负极上金属失电子生成金属阳离子进入溶液而被腐蚀,较不活泼的金属作正极而不易腐蚀,B不易腐蚀,所以金属活动性A>B;金属和酸反应,较活泼的金属与酸反应较剧烈,将A、D分别投入等浓度盐酸中,D比A反应剧烈,所以金属活动性D>A;金属之间的置换反应中,较活泼金属能置换出较不活泼的金属,将铜浸入B的盐溶液里,无明显变化,所以金属活动性:B>Cu;如果把铜浸入C的盐溶液里,有金属C析出,说明金属活动性:Cu>C。所以它们的活动性由强到弱的顺序是D>A>B>C,故合理选项是B。
3.由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是( C )