水是弱场配体。在六个水分子的八面体场中,金属离子Ti3+中的5个d轨道分裂成两组:低能T2g(dxy,dxz,dyz);高能Eg(dz2,dx2-y2)。由于Ti3+只有一个电子,这个电子将落在低能T2g组里。
由于这两组轨道的能量差正好和可见光光谱中的黄绿色光的光子能量相同,在可见光的照射下,处在低能级轨道上的电子将会吸收(黄绿色光)能量,同时发生跃迁(到高能级的Eg)。这样,照射在配离子上的白色的可见光缺少了黄绿色的成分,就会显示出黄绿色的“互补光”颜色---紫色。
所以,Ti(H2O)63+显紫色
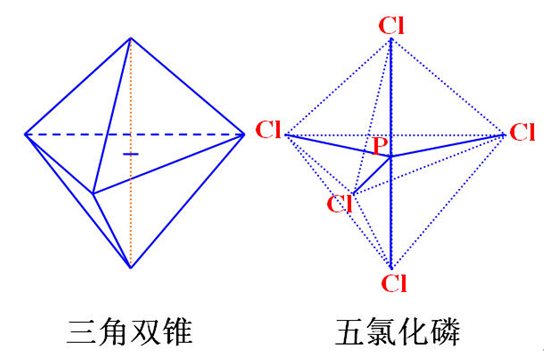
三角双锥构型,中间是一个正三角形。但是不能选取其他的平面正三角形平面了,所以并不是完美对称图形。
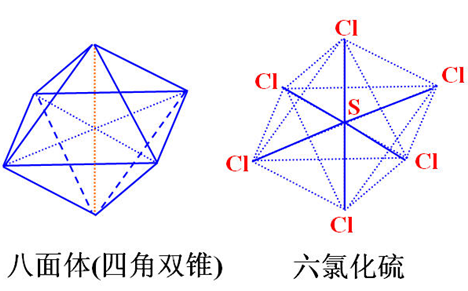
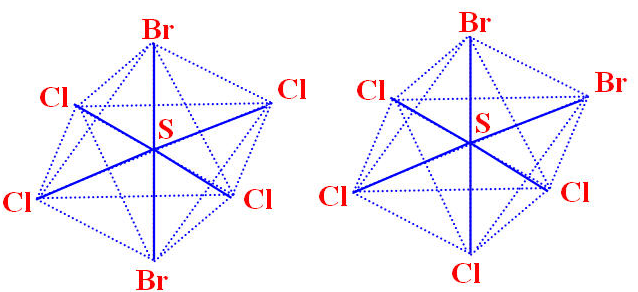
正八面体构型,中间是一个正方形;选取另外一个面,也是正方形。所以是完美对称的结构SCl5Br有及几种结构?思路:正八面体是完美对称结构,所以只有一种一氯代物
SCl4Br2有及几种结构?
思路:取代第一个只有1种;取代第二个有几种呢?其实有两种,分别是相邻的以及相对的