
提示:多个视频只播放第一个文件,完整视频请下载后播放。
【视频+教学设计+课件】高中化学大单元教学优质课比赛鲁科版选择性必修2第二章《配位键》第2课时《配位平衡》宿城一中 李航
宿城一中 李航 指导老师:陈诚 程波)










一、教学内容分析
1.内容分析
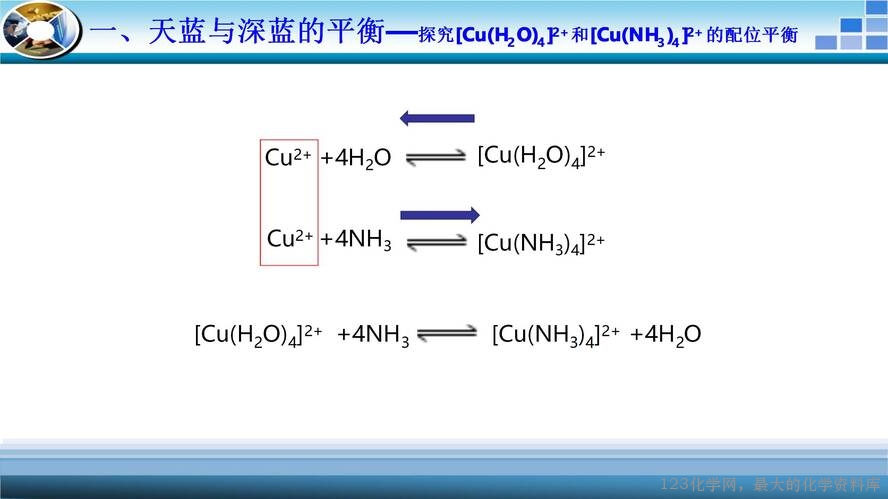
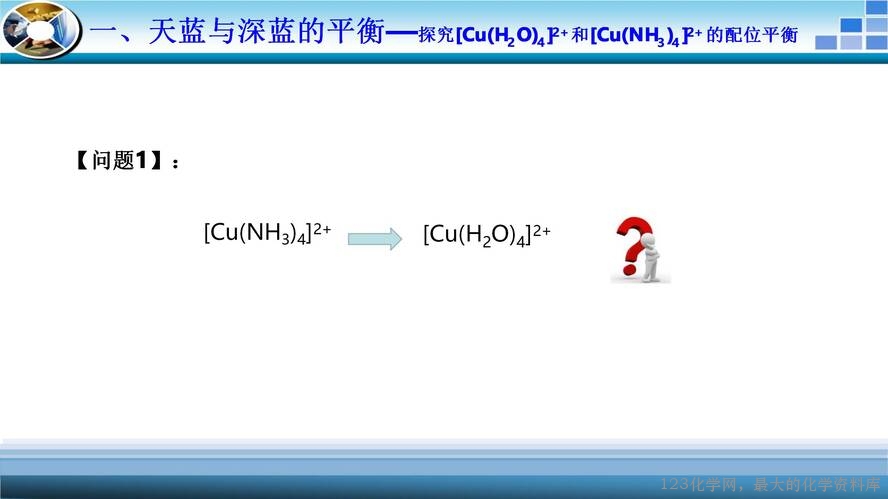
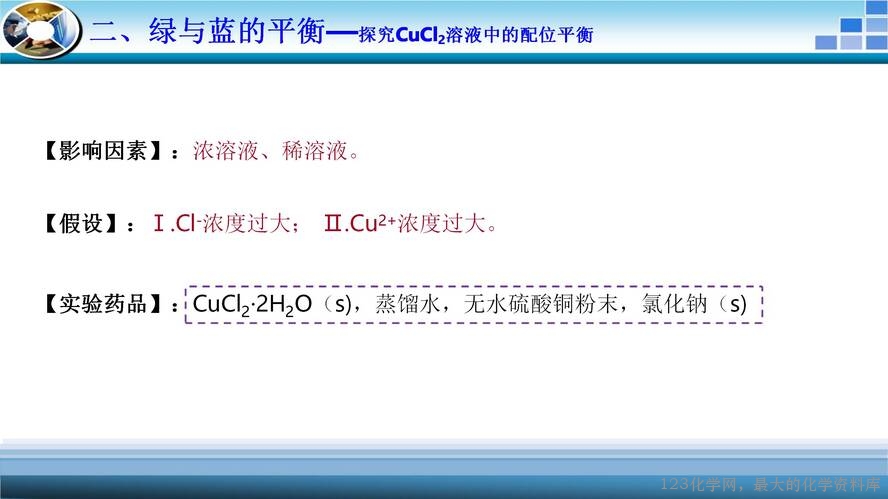
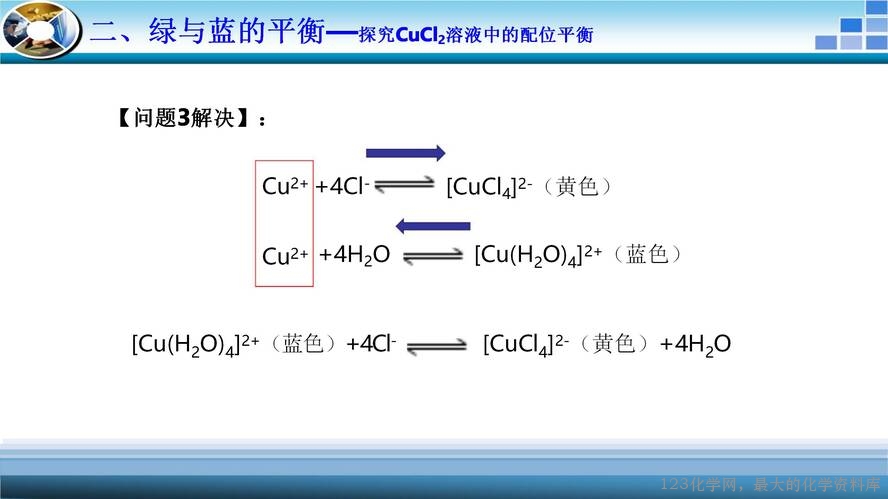
本节课的核心是配位平衡,通过实验加深学生对配位平衡的理解。以[Cu(H2O)4]2+转变为[Cu(NH3)4]2+提到配合物内界的电离以及配位平衡移动的基本概念。接着反问学生[CuNH3)4]2+能不能转化为[Cu(H2O)4]2+并施以实验验证,实验现象与预期现象出现矛盾,学生提出加酸的优化方案,再次实验,发现加硫酸和盐酸现象不同,并且盐酸浓度不同,现象也不一样,原因何在?氯化铜溶液一定呈绿色吗?向氯化铜固体中加少量水溶液呈绿色,接着再加水,溶液转变为天蓝色,从配位平衡的角度给予学生解释。在此基础上,引导学生自行解释[Cu(NH3)4]2+溶液加硫酸和盐酸现象不同且盐酸浓度不同,现象也不一样的原因。
最后学生学以致用,利用配位平衡解释生活中的一些现象,加深对配位平衡的理解。
2.素养呈现
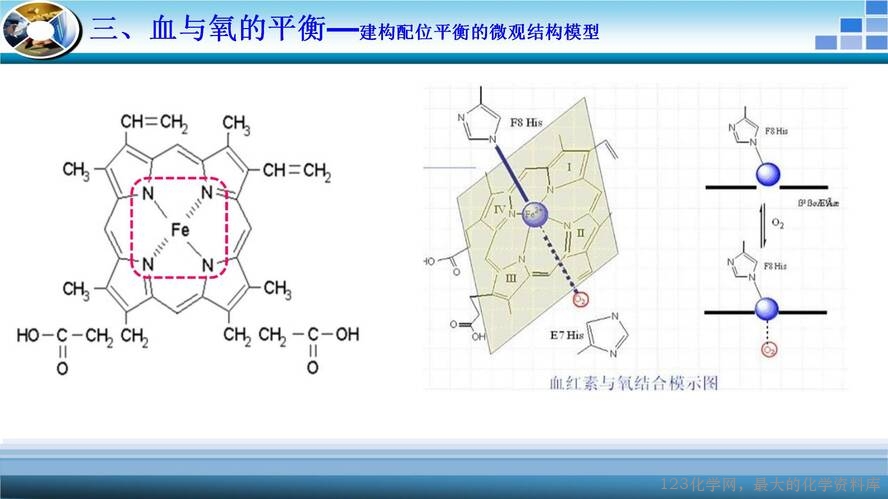
微观粒子决定物质宏观呈现颜色,[Cu(H2O)4]2+、[Cu(NH3)4]2+、[CuCl4]2-三种微粒分别呈天蓝色、深蓝色、黄色;同时在实验过程中,通过溶液颜色不断地改变,引导学生建立平衡思想来解决问题;实验过程中出现的实验现象与预期矛盾,引导学生建立观点、科学探究,以此发展学生“宏观辨识与微观探析”“变化观念与平衡思想”“科学探究与创新意识”等核心素养。
二、对学情的思考
已有知识:学习过配位键的基础概念,银氨溶液的配制等等。
局限认识:只限于表面,把他们作为特殊的现象进 了重点记忆,对其中的原因进 了回避。
发展方向:本节通过配位平衡的学习,将打开并诠释学生封沉已久的困惑。
三、教学目标
1.运用“控制变量”思想,通过实验探究配位平衡移动原理,能从配位平衡移动角度解释实验现象。
2.通过实验探究,理解浓度、压强等对配位平衡状态的影响,进一步建构“化学变化是有条件的”这一学科观念;
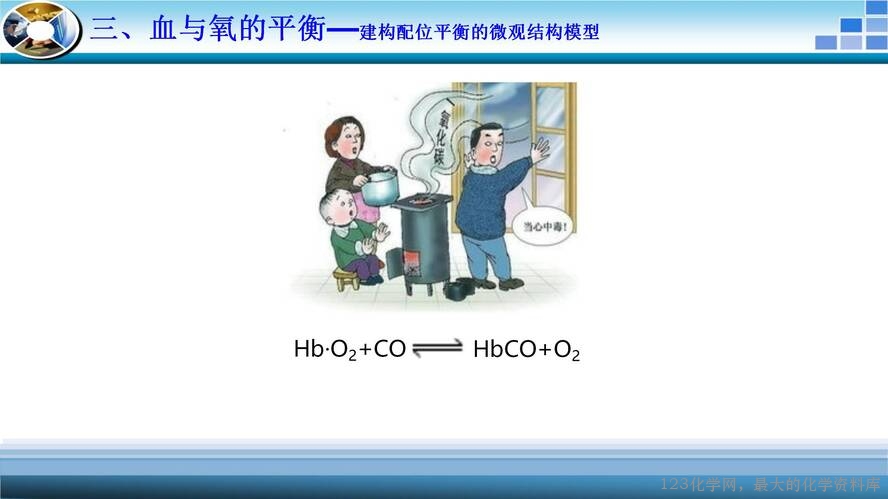
3.能运用配位平衡移动原理解释生产生活中的一些实例。
四、教学方法:实验法、讨论法