
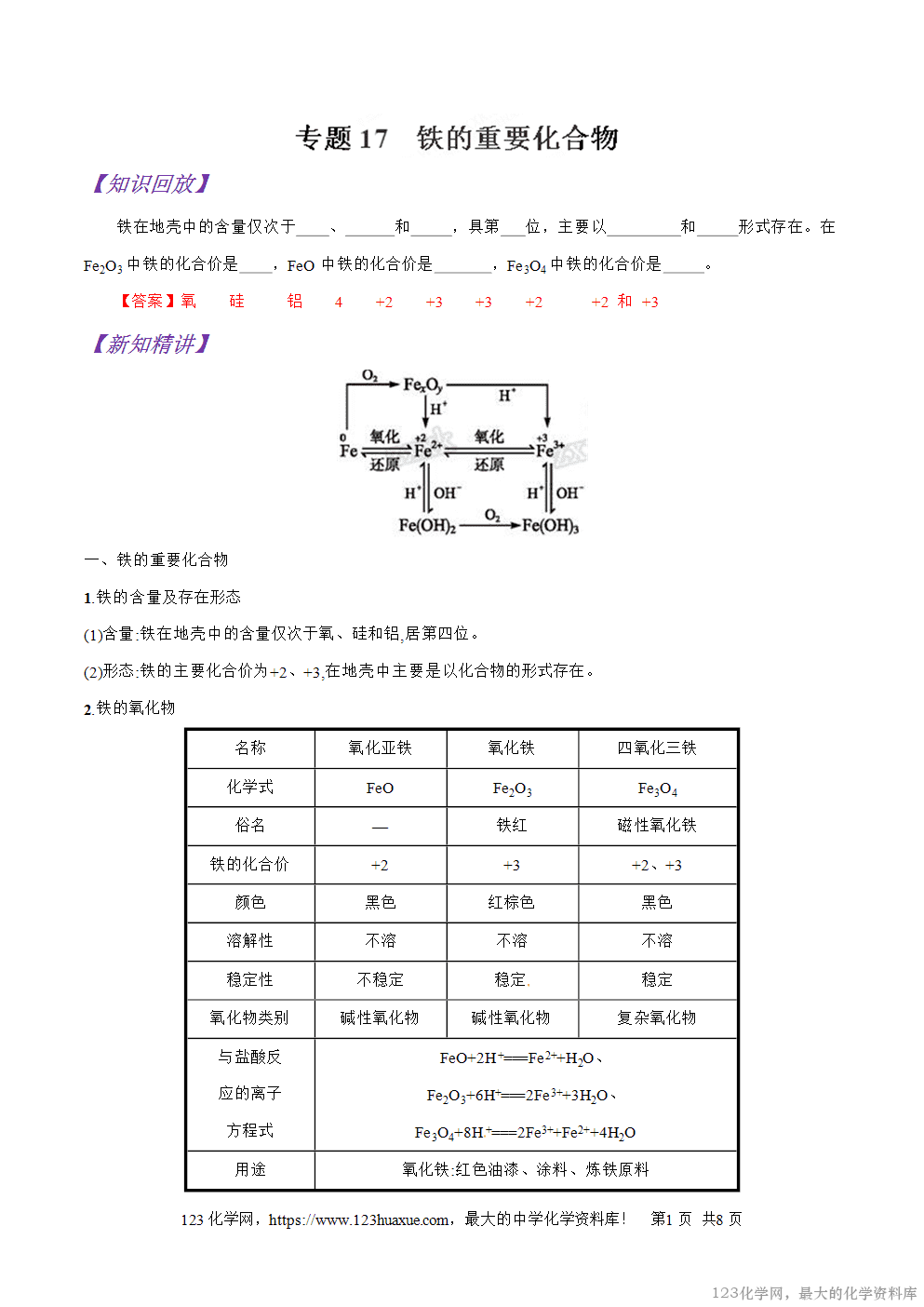

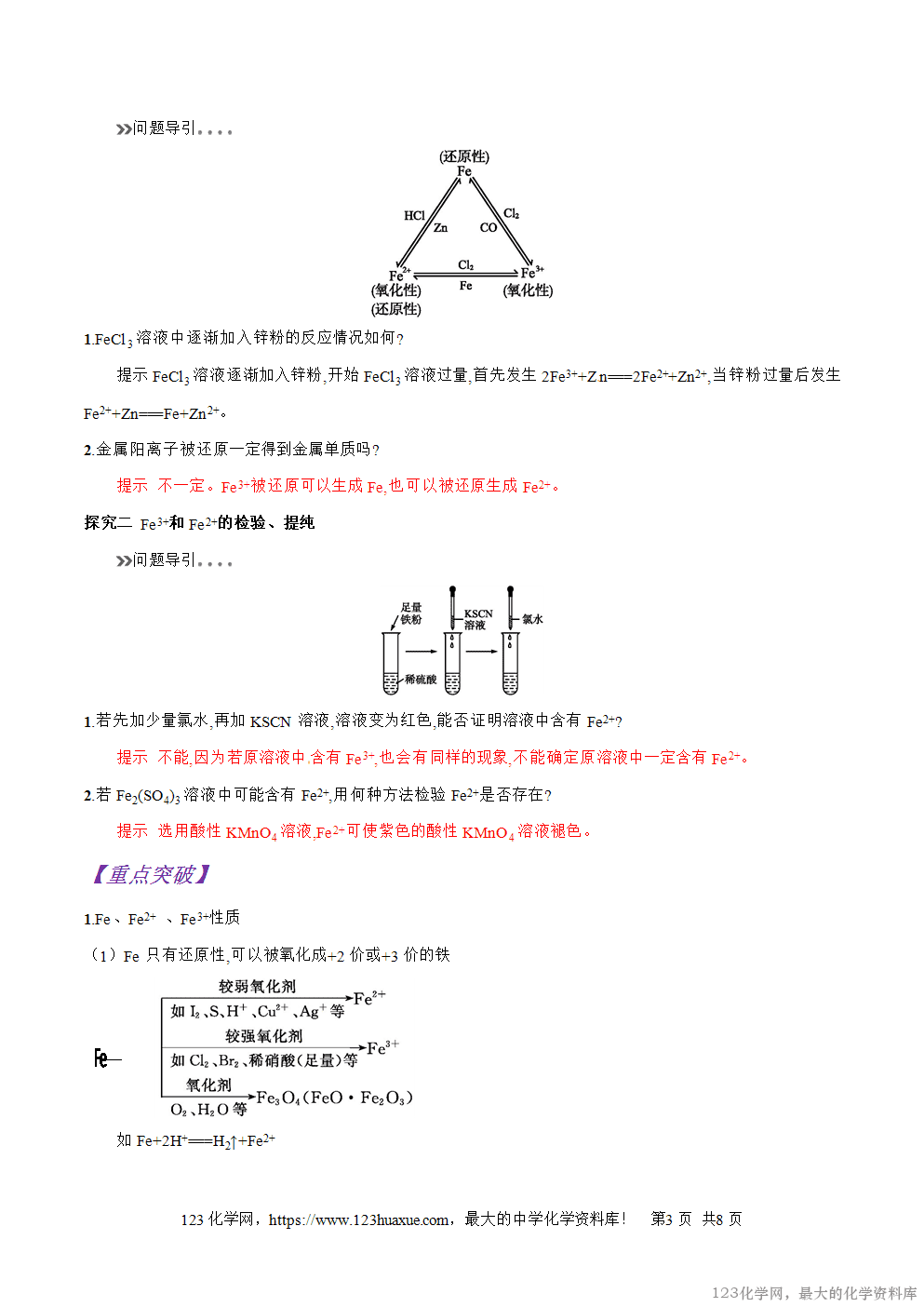
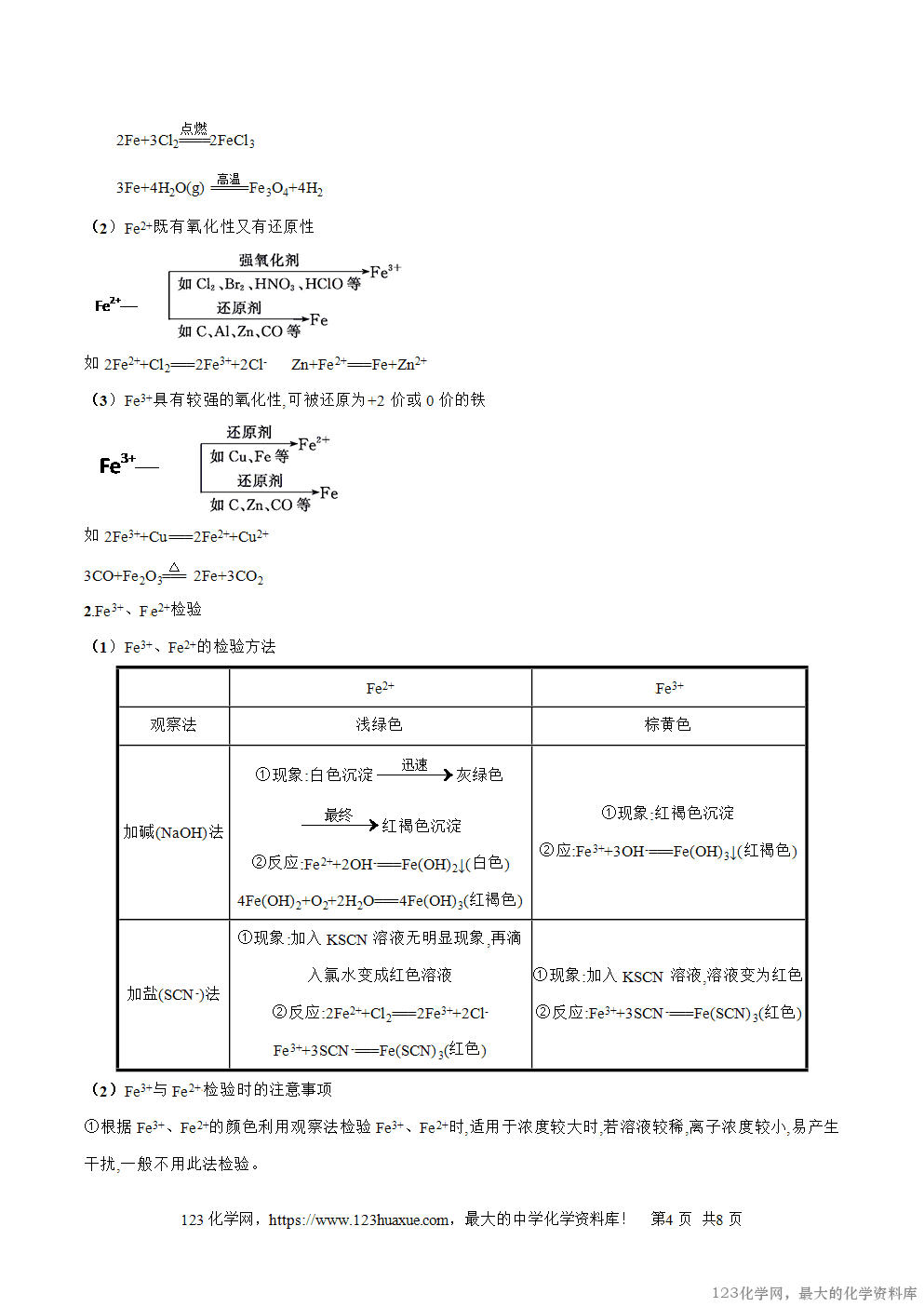
探究一 “铁三角”的转化关系分析
问题导引
1.FeCl3溶液中逐渐加入锌粉的反应情况如何?
提示FeCl3溶液逐渐加入锌粉,开始FeCl3溶液过量,首先发生2Fe3++Zn===2Fe2++Zn2+,当锌粉过量后发生Fe2++Zn===Fe+Zn2+。
2.金属阳离子被还原一定得到金属单质吗?
提示 不一定。Fe3+被还原可以生成Fe,也可以被还原生成Fe2+。
探究二 Fe3+和Fe2+的检验、提纯
问题导引
1.若先加少量氯水,再加KSCN溶液,溶液变为红色,能否证明溶液中含有Fe2+?
提示 不能,因为若原溶液中含有Fe3+,也会有同样的现象,不能确定原溶液中一定含有Fe2+。
2.若Fe2(SO4)3溶液中可能含有Fe2+,用何种方法检验Fe2+是否存在?
提示 选用酸性KMnO4溶液,Fe2+可使紫色的酸性KMnO4溶液褪色。
【重点突破】
1.Fe、Fe2+ 、Fe3+性质
(1)Fe只有还原性,可以被氧化成+2价或+3价的铁
如Fe+2H+===H2↑+Fe2+
2Fe+3Cl2点燃====2FeCl3
3Fe+4H2O(g) 高温=====Fe3O4+4H2
(2)Fe2+既有氧化性又有还原性
如2Fe2++Cl2===2Fe3++2Cl- Zn+Fe2+===Fe+Zn2+
(3)Fe3+具有较强的氧化性,可被还原为+2价或0价的铁
如2Fe3++Cu===2Fe2++Cu2+
3CO+Fe2O3△=== 2Fe+3CO2
2.Fe3+、Fe2+检验
(1)Fe3+、Fe2+的检验方法