1.三种分散系的本质区别
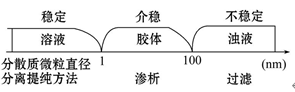
(1)分散系中至少含有两种物质,都属于混合物,蒸馏水不是一种分散系
(2)三种分散系之间的转化为物理变化
(3)透明不代表无色,如CuSO4溶液为蓝色溶液,Fe(OH)3胶体为红褐色液体。
(4)胶体不一定都呈液体,胶体除了液溶胶还有气溶胶和固溶胶。
2.胶体的性质
(1)外观:较均一、较透明、较稳定
(2)通透性:能透过滤纸,不能透过半透膜
(3)电学特性:胶不带电荷
3.常见胶体
(1)气溶胶:云、烟、雾
(2)液溶胶:豆浆、氢氧化铝胶体、Fe(OH)3胶体、硅酸胶体
(3)固溶胶:果冻、宝石、烟水晶、有色玻璃
(4)三种有机胶体:淀粉溶液、肥皂溶液、蛋白质溶液
4.鉴别胶体和溶液
(1)方法:丁达尔效应
(2)操作:用可见光束照射,看在入射光侧面是否看到一条光亮的“通路”
5.胶体的聚沉
(1)现象:胶体形成沉淀析出的现象
(2)变化:物理变化
(3)方法
①加入电解质溶液
②加入带相反电荷胶粒的胶体
③加热或搅拌
(4)Fe(OH)3胶体滴加盐酸至过量现象先产生红褐色沉淀,后沉淀全部溶解
6.胶体的吸附性:胶体的比表面积大,吸附能力强
7.胶体的电泳
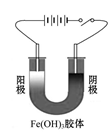
(1)概念:在外电场的作用下胶体微粒发生定向移动
(2)原因:胶体微粒比表面积大,吸附能力强,吸附了带电离子而带电荷
(3)规律:带正电荷的胶粒向阴极移动,带负电荷的胶粒向阳极移动
(4)变化:发生化学变化(电解反应)
8.胶体的形成
(1)形成过程:将纳米颗粒分散到适当的分散剂中形成的一种分散系
(2)结构特点:胶粒是高分子或多分子聚合体
①胶体中所含胶粒的个数不确定
②胶粒所带的电荷数不确定
(3)淀粉胶体的特殊性
①结构特征:淀粉胶体为分子胶体,胶粒不带电荷
②性质特性:加入电解质溶液不能发生聚沉,通电后不能发生电泳
9.Fe(OH)3胶体的制备和分离提纯
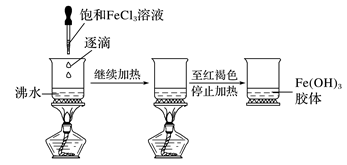
(1)制备
①原理:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
②操作:向沸水中滴加饱和FeCl3溶液,至液体呈透明的红褐色,停止加热
(2)除去胶体中所含杂质
①胶体中的悬浊液:过滤
②胶体中的分子或离子:渗析
(3)实验方法证明Fe(OH)3胶体和Cl-两者已经分离完全:取最后一次渗析液与结晶的试管中,加入硝酸银溶液,若无白色沉淀产生,则说明两者已经完全分离
10.胶体的应用
(1)胶体的聚沉
①卤水点豆腐
②河海交界处容易形成三角洲
③FeCl3溶液常用作凝血剂
(2)胶体的吸附性
①明矾、Fe2(SO4)3溶液净水
②Al(OH)3胶体作漂白剂
(3)胶体的丁达尔现象
①清晨阳光穿过茂密树木枝叶产生的美丽光线
②电影院光柱
③海市蜃楼
【误区警示】
(1)丁达尔效应是物理变化而不是化学变化。
(2)明矾作净水剂是利用明矾溶于水生成Al(OH)3胶体,胶体具有吸附性;但胶体没有杀菌消毒的作用。
(3)胶体呈电中性,不带电荷。而胶粒可能带正电荷或负电荷或不带电荷。