配合物的组成
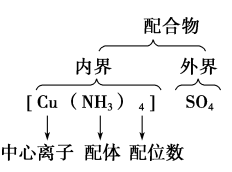
一般中心原子(或离子)的配位数是2、4、6。
①中心离子
配合物的中心离子一般都是带正电的阳离子,过渡金属离子最常见,但也有呈电中性的原子,甚至还有极少数的阴离子;
②配体
配体可以是阴离子,如X-(卤素离子)、OH-、SCN-、CN-、RCOO-(羧酸根离子)、C2O4(2-)、PO43-等;也可以是中性分子,如H2O、NH3、CO、醇、胺、醚等。配体中直接同中心离子(或原子)配合的原子叫作配位原子。配位原子必须是含有孤电子对的原子,如NH3中的氮原子、H2O中的氧原子,配位原子常是ⅤA族、ⅥA族、ⅦA族的元素原子;
③内界和外界
配合物分为内界和外界,其中配离子称为内界,与内界发生电性匹配的阳离子或阴离子称为外界,外界和内界以离子键相结合;
④配位数
直接同中心离子(或原子)配位的原子的数目叫中心离子(或原子)的配位数。要注意只含有一个配位原子的配体称为单基配体,中心离子同单基配体结合的数目就是该中心离子的配位数,如[Fe(CN)6]4-中Fe2+的配位数为6。含有两个以上配位原子的配体叫多基配体,中心离子(或原子)同多基配体配合时,配位数等于同中心离子配位的原子数,如乙二胺分子中含有两个配位氮原子,故在[Pt(en)2]Cl2(其中,en代表乙二胺分子)中Pt2+的配位数为2×2=4,而配体只有两个。
(2)形成配合物的条件
①配体有孤电子对;
②中心原子(或离子)有空轨道。
(3)配合物溶于水的电离情况
配合物中外界离子能电离出来,而内界离子不能电离出来,通过实验及其数据可以确定内界和外界离子的个数,从而可以确定其配离子、中心离子和配体。
(4)配离子的电荷数
配离子的电荷数等于中心离子和配体总电荷的代数和。