
提示:多个视频只播放第一个文件,完整视频请下载后播放。
授课教师:安徽省五河第一中学 马其杰
碧水计划之废水处理中的沉淀溶解平衡问题
第3课时 沉淀溶解平衡的应用











环节一:探究氢氧化铜转化为氢氧化镁的可能性
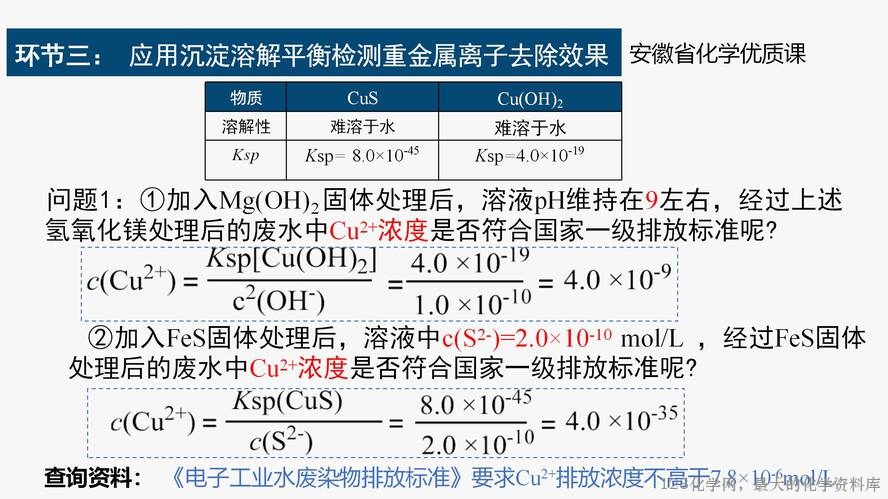
复习引入:前两节课的学习中我们知道了难溶电解质氢氧化镁在废水处理中扮演了重要的的 角色,不但可以中和酸性废水,还可以通过沉淀转化除去体系中重金属离子(Cu2+),实验 中能明显观察到蓝色沉淀,与我们计算的转化平衡常数 K=1.0 ×108 理论上吻合,证实反应可 以进行, 并且程度很大。据此我们知道难溶物可以向更难溶的方向转化, 程度可以通过反应 的平衡常数 K 进行定量判断。溶解度小的可不可以向溶解度大的方向转化呢?下面我们仍 然以氢氧化铜和氢氧化镁为例,探究这个溶解平衡能否反向进行。
问题 1:氢氧化铜能转化为氢氧化镁吗?
活动 1:学生讨论后回答。预测①能, Mg2+ 能结合氢氧化铜溶解产生的 OH-离子,使氢氧化 铜平衡向溶解方向进行, 使氢氧化镁平衡向沉淀方向进行, 最终完成转化。②不能。氢氧化 铜的 Ksp 更小, Cu2+结合 OH-离子的能力和程度更大。即镁离子不能使沉淀转化向着生成氢 氧化镁的方向移动。
评价 1:教师根据学生回答的情况进行引导,氢氧化铜中是否存在溶解平衡?镁离子加入能 否影响平衡?影响的结果是什么?从而得出微观上可能会完成转化。并评价学生对物质溶解 平衡及其移动的掌握情况。
问题 2:依据前面经验,我们该如何设计试验验证氢氧化铜能否转化为氢氧化镁?
活动 2:小组讨论,由小组代表交流讨论结果,并互相评价。再分工合作,根据提供的仪器
和药品,设计实验方案。共同完成氢氧化铜能否转化为氢氧化镁的探究。
环节二:应用转化平衡探索新废水处理剂的可行性
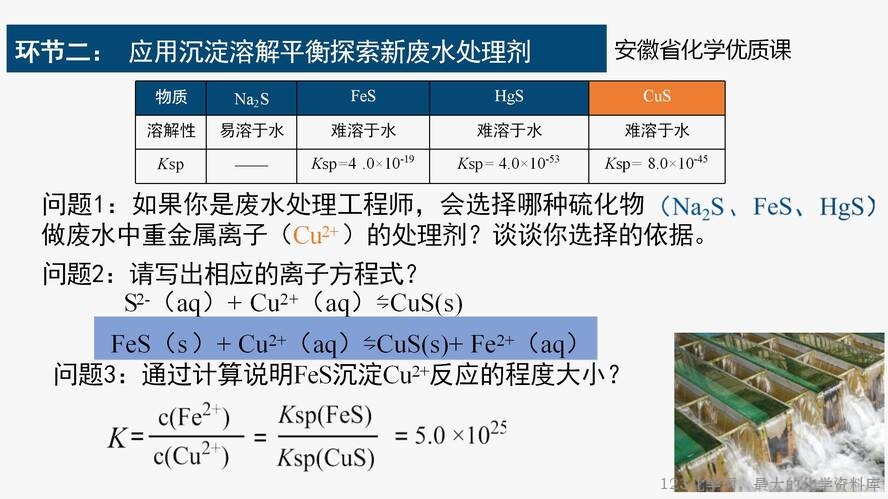
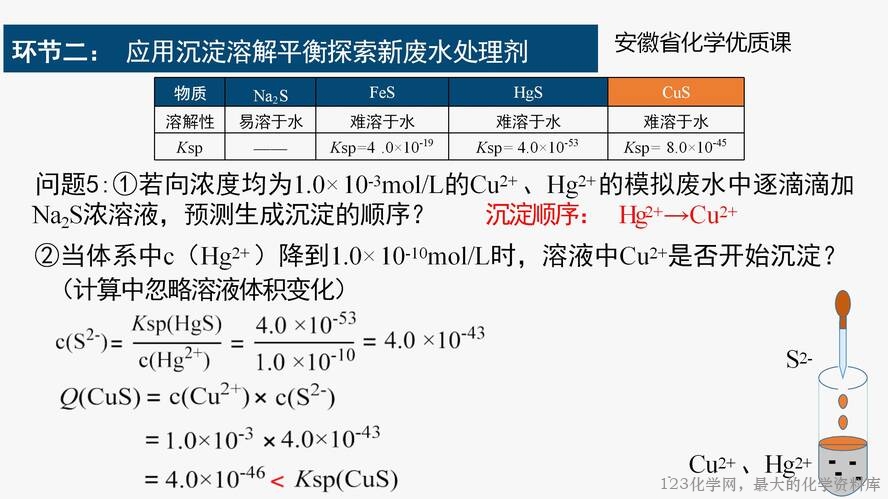
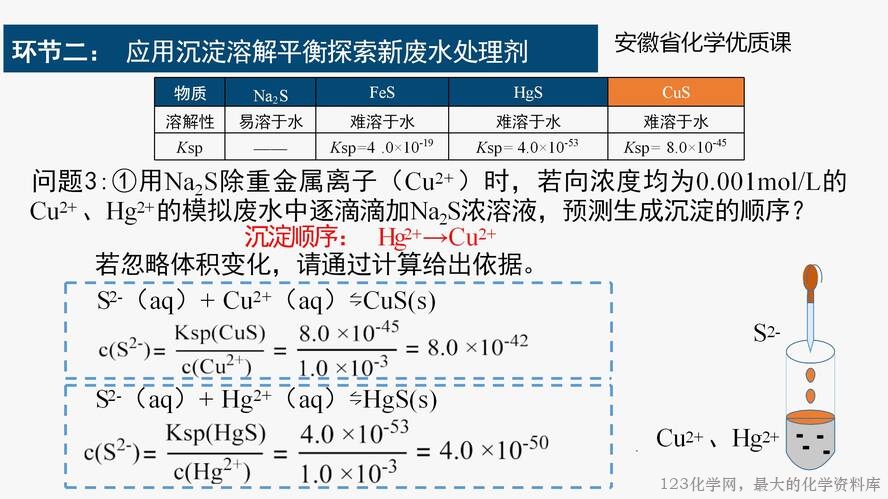
问题 5:依据文献,废水中重金属离子也可以用硫化物处理,如果你是废水处理工程师,选 择哪种硫化物(Na2S 、FeS 、HgS)做废水中重金属离子(Cu2+ )的处理剂?从物质溶解性 的角度、结合沉淀转化规律谈一谈你的想法。
活动 5:学生思考、交流。水体中沉淀 Cu2+ 的本质是 S2-(aq)+ Cu2+(aq)⇋CuS(S),分析
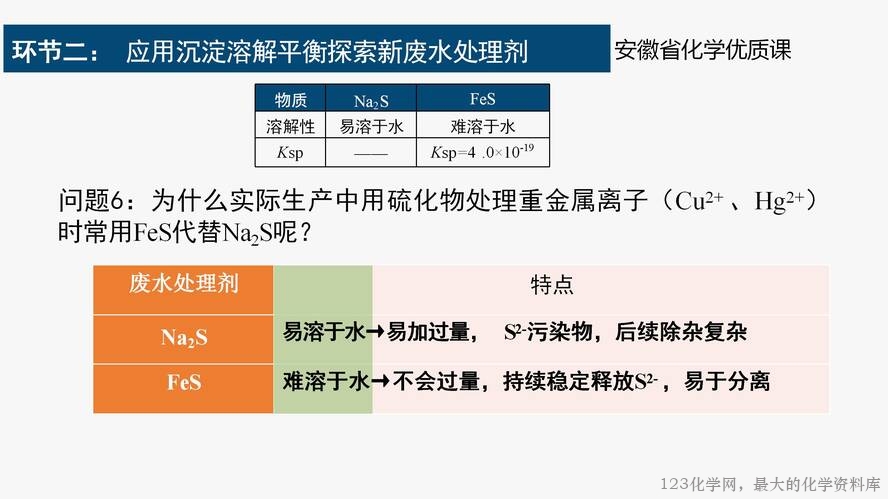
平衡移动结果可能的答案:①硫化汞溶解度最小,溶解产生的 S2-(aq)最小,沉淀二价铜 困难,即沉淀由溶解度大的向溶解度小的方向转化困难,此外 HgS 溶解产生的 Hg2+也是重 金属离子,依据除杂原理,不能向水体中引入新的重金属离子,故不能选择;②可以选择硫 化钠,溶解度大,即溶解产生的硫离子浓度大,离子溶度更容易达到 CuS 的 Ksp 从而达到 除去 Cu2+ 的目的;③硫化亚铁溶解度(Ksp)比硫化铜大(Ksp),依据沉淀转化原理,可以 实现硫化亚铁向更难溶的硫化铜的转化,从而达到除去 Cu2+ 的目的,同时自身在水体中难 溶解,便于后期分离除去。
评价 5:在新情景新任务里诊断学生难溶电解质学习掌握情况。评价学生对前两节课所学习 的沉淀溶解平衡转化的知识掌握情况, 并分析学生知识迁移的能力, 为下一阶段具体的硫化 物除杂做好准备。
问题 6:接下来我们按照寻找平衡、定量平衡、分析平衡、结果判断的步骤开展研究。
若使用硫化亚铁和硫化钠沉淀废水中的 Cu2+ ,分别对应的离子方程式分别是什么?活动 6:
学生独立思考后书写回答。①S2-(aq)+ Cu2+(aq)⇋CuS(s)②FeS(s)+ Cu2+(aq)⇋CuS(s)+
Fe2+(aq)
评价 6:围绕从已有的方程式知识开展师生互评活动,分析学生书写过程中的问题,引导发 现方程式物质状态说明的重要性及意义。评价学生书写方程式的能力。
问题 7:通过计算平衡常数说明硫化亚铁转化为硫化铜的平衡常数?
活动 7:学生依据经验通过两难溶物 Ksp 比值计算转化平衡常数。