




















(2025·广东卷)CuCl微溶于水,但在浓度较高的溶液中因形成和而溶解。将适量CuCl完全溶于盐酸,得到含和的溶液,下列叙述正确的是
A.加水稀释,浓度一定下降
B.向溶液中加入少量NaCl固体,浓度一定上升
C.的电离方程式为:
D.体系中,
【答案】A
【解析】A.加水稀释,溶液体积变大,浓度一定下降,A正确;
B.加入NaCl会增加Cl⁻浓度,可能促使转化为,浓度不一定上升,B错误;
C.H[CuCl2]应电离为H+和,而非分解为Cu+和Cl-,电离方程式错误,C错误;
D.电荷守恒未考虑的电荷数,电荷守恒应为,D错误;
故选A。
2.(2025·浙江1月卷)时,的电离常数。下列描述不正确的是
A.
B.
C.
D.溶液中,,则
【答案】D
【解析】A.,K==,A正确;
B.,K==,B正确;
C.,K==,C正确;
D.=,由于,,D错误;
答案选D。
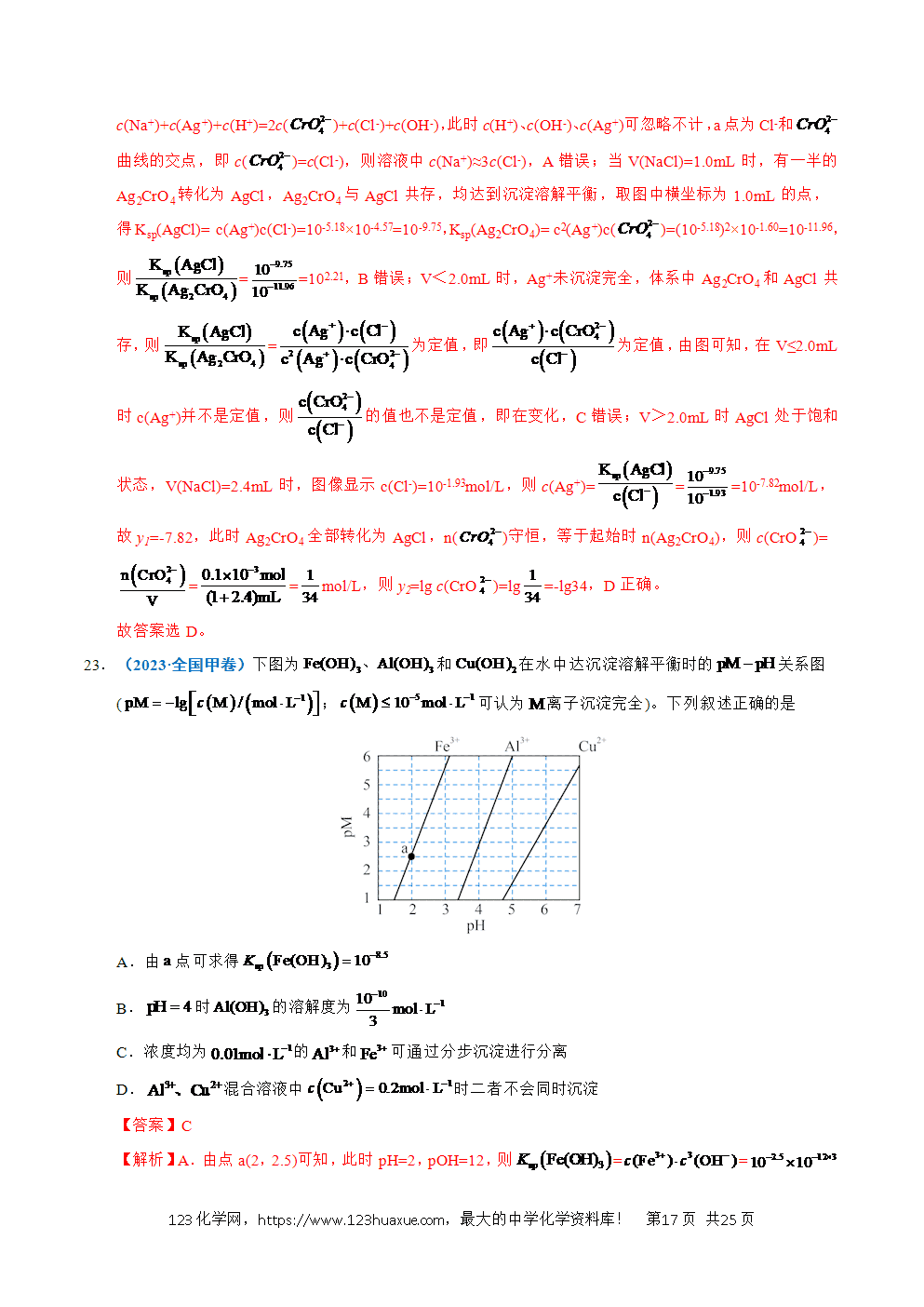
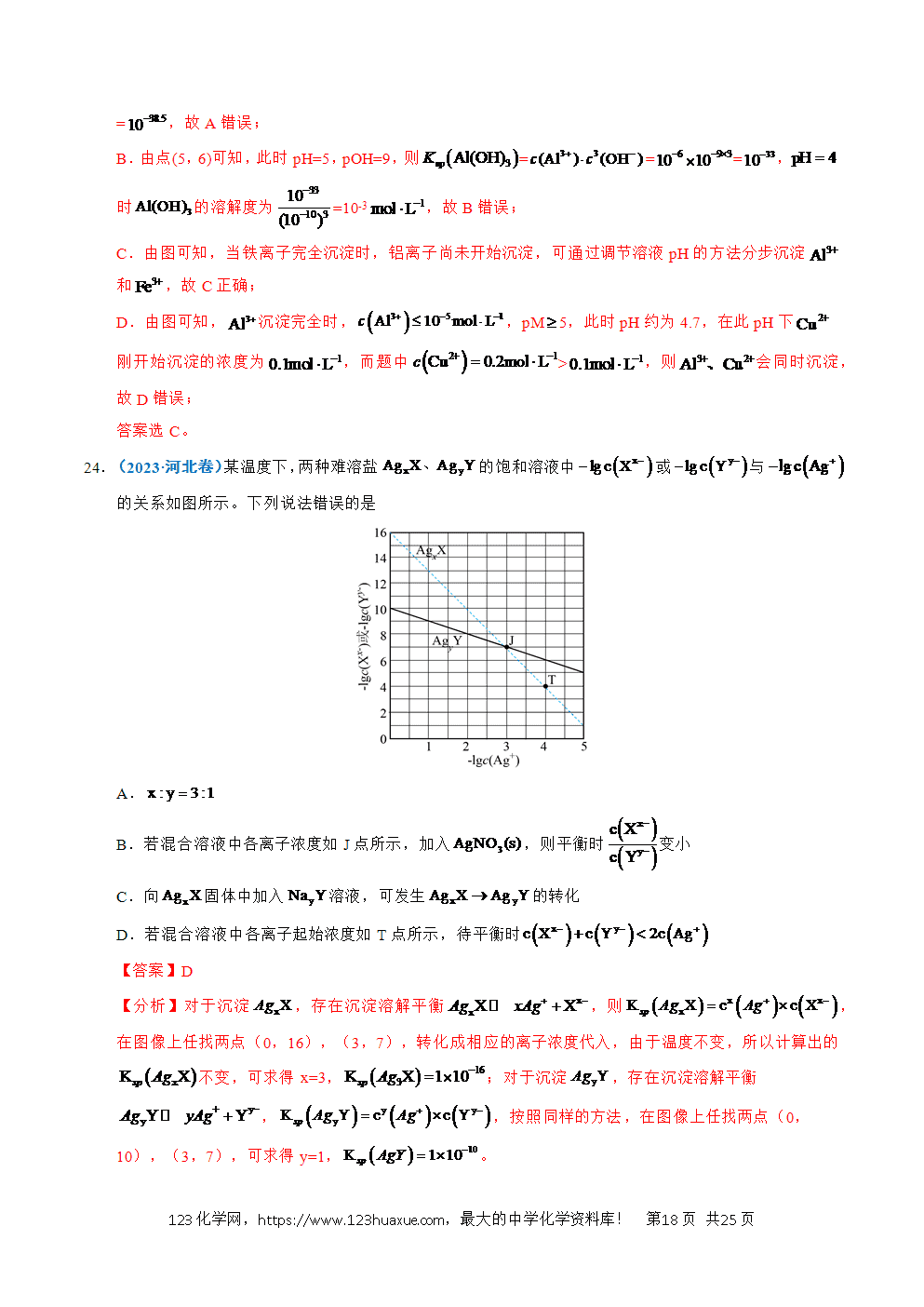
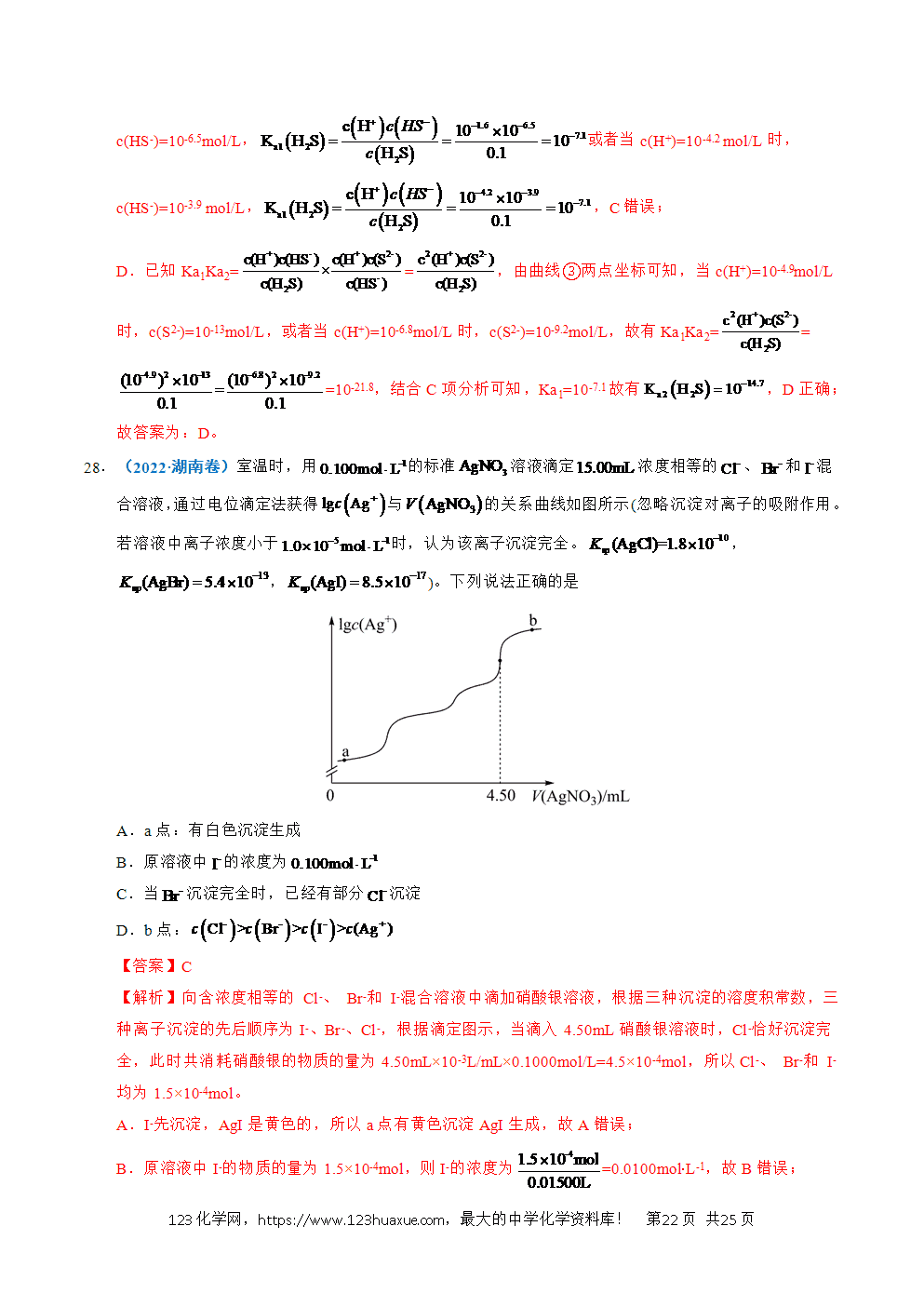
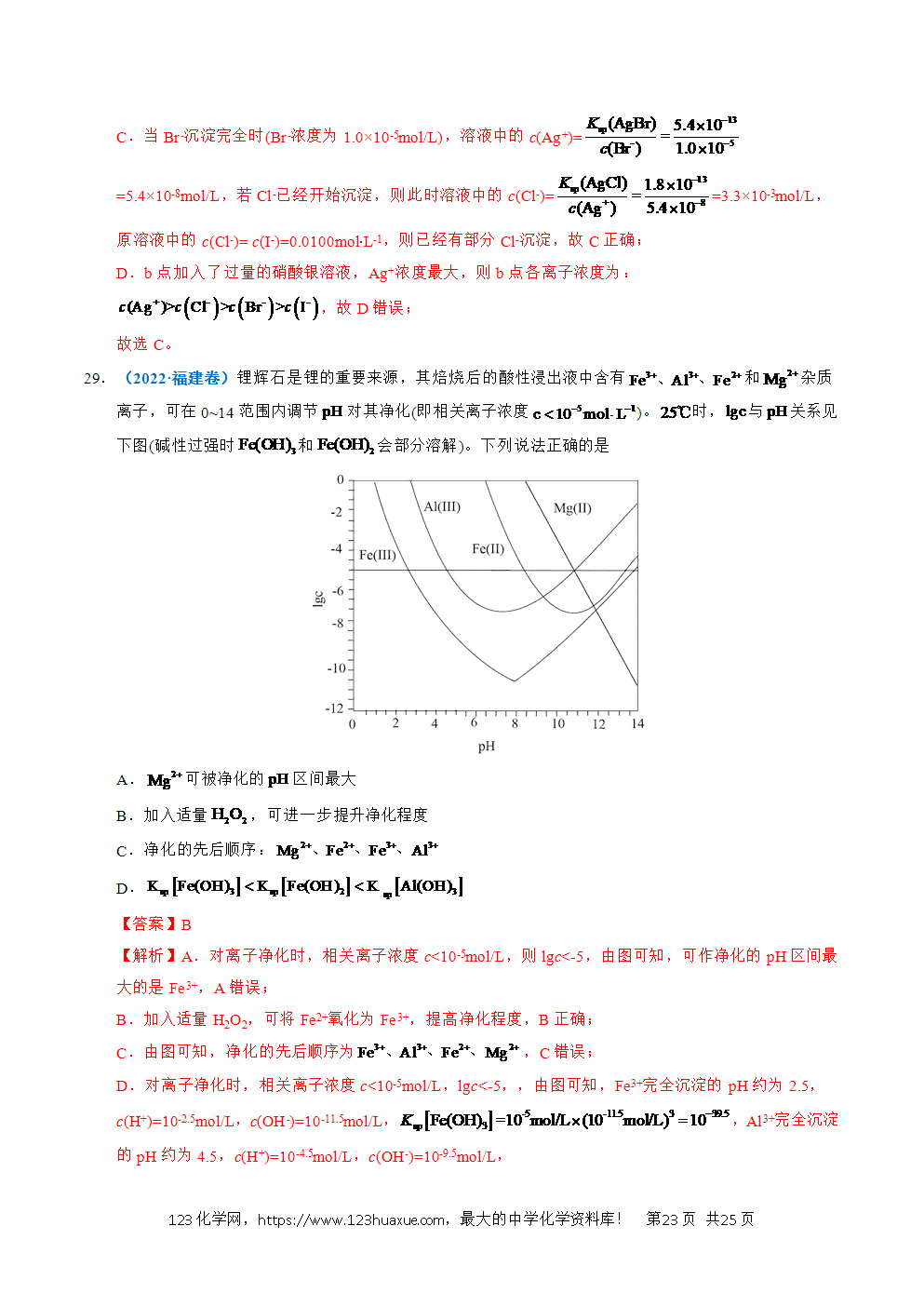
3.(2024·江苏卷)室温下,通过下列实验探究的性质。已知,。
实验1:将气体通入水中,测得溶液。
实验2:将气体通入溶液中,当溶液时停止通气。
实验3:将气体通入酸性溶液中,当溶液恰好褪色时停止通气。
下列说法正确的是
A.实验1所得溶液中:
B.实验2所得溶液中:
C.实验2所得溶液经蒸干、灼烧制得固体
D.实验3所得溶液中:
【答案】D
【分析】实验1得到H2SO3溶液,实验2溶液的pH为4,实验2为NaHSO3溶液,实验3和酸性溶液反应的离子方程式为:。
【解析】A. 实验1得到H2SO3溶液,其质子守恒关系式为:,则 ,A错误;
B.实验2为pH为4,依据,则=,溶液,则,B错误;
C.NaHSO3溶液蒸干、灼烧制得固体,C错误;
D.实验3依据发生的反应:,则恰好完全反应后,D正确;
故选D。