水解常数与电离平衡常数
(1)水解常数的概念
在一定温度下,能水解的盐(强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐)在水溶液中达到水解平衡时,生成的弱酸(或弱碱)浓度和氢氧根离子(或氢离子)浓度之积与溶液中未水解的弱酸根阴离子(或弱碱的阳离子)浓度之比是一个常数,该常数就叫水解平衡常数。
(2)水解常数(Kh)与电离常数的定量关系
①强碱弱酸盐如CH3COONa溶液:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-

③NaHCO3的水解常数Kh=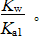
水解常数与电离平衡常数的区别与联系
分类:3-3盐类的水解 日期: 点击:0
水解常数与电离平衡常数
(1)水解常数的概念
在一定温度下,能水解的盐(强碱弱酸盐、强酸弱碱盐或弱酸弱碱盐)在水溶液中达到水解平衡时,生成的弱酸(或弱碱)浓度和氢氧根离子(或氢离子)浓度之积与溶液中未水解的弱酸根阴离子(或弱碱的阳离子)浓度之比是一个常数,该常数就叫水解平衡常数。
(2)水解常数(Kh)与电离常数的定量关系
①强碱弱酸盐如CH3COONa溶液:CH3COO-+H2O CH3COOH+OH-
CH3COOH+OH-

③NaHCO3的水解常数Kh=