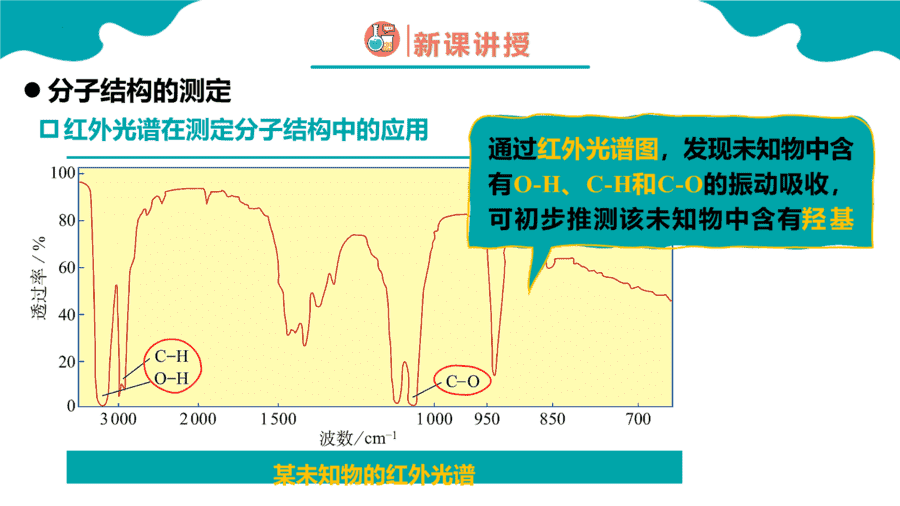
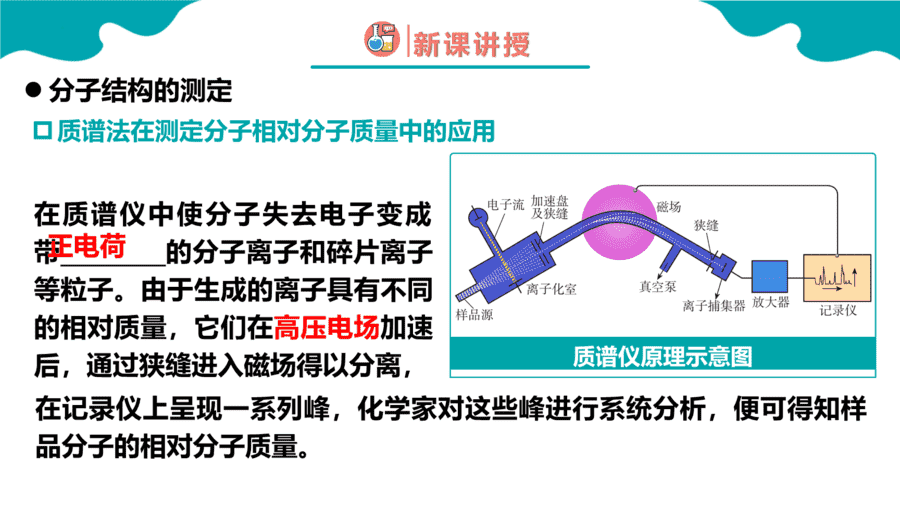
1.下列对分子结构的描述,正确的是
A.O原子发生杂化
B.O原子与、都形成键
C.该分子为直线形分子
D.分子的结构式是:
【答案】B
【详解】A.HClO中O原子形成2个σ键,含有2个孤电子对,价层电子对数为4,采用sp3杂化,故A错误;
B.中O原子与H形成O-H键,与Cl形成O-Cl键,单键都是键,因此O原子与、都形成键,故B正确;
C.HClO的中心原子O原子采用sp3杂化,含有2个孤电子对,则其空间构型为V形,故C错误;
D.的中心原子是O原子,则其结构式为H-O-Cl,故D错误;
故答案选B。
2.是一种常见的还原剂,可通过如下反应制备。下列说法错误的是
A.该反应在无水环境下进行
B.该反应是氧化还原反应
C.元素的第一电离能:
D.的空间构型为正四面体形
【答案】B
【详解】A.NaH会和水反应,故该反应在无水环境下进行,A正确;
B.该反应中不存在元素化合价的改变,不是氧化还原反应,B错误;
C.同一主族随原子序数变大,原子半径变大,第一电离能变小;同一周期随着原子序数变大,第一电离能变大,元素的第一电离能:,C正确;
D.中B形成4个共价键,为sp3杂化,空间构型为正四面体形,D正确;
故选B。
3.CsCl是一种分析试剂,制备方法。下列说法正确的是
A.CsCl的电子式: B.基态的核外电子排布式:
C.的空间构型:三角锥形 D.中子数为18的Cl原子: