



第Ⅰ卷
一、选择题:本题共30小题,每小题2分,共60分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列做法值得提倡的是
A.生活垃圾焚烧处理 B.出门乘坐公共交通
C.实验室废水直接倒入下水道 D.为果蔬除虫,大量使用农药
【答案】B
【详解】A.焚烧会产生有害气体和颗粒物,可能造成空气污染,A不符合题意;
B.公共交通可减少私家车使用,降低能源消耗和碳排放,符合环保理念,值得提倡,B符合题意;
C.实验室废水含化学污染物,直接排放会污染水源,必须经处理后排放,C不符合题意;
D.农药残留会危害健康,污染环境,应合理使用或采用生物防治等替代方法,D不符合题意;
故选B。
2.氧有三种天然同位素O、O、O,在地球科学、气候研究和考古学中有广泛应用。其中核素O的中子数是
A.8 B.17 C.9 D.25
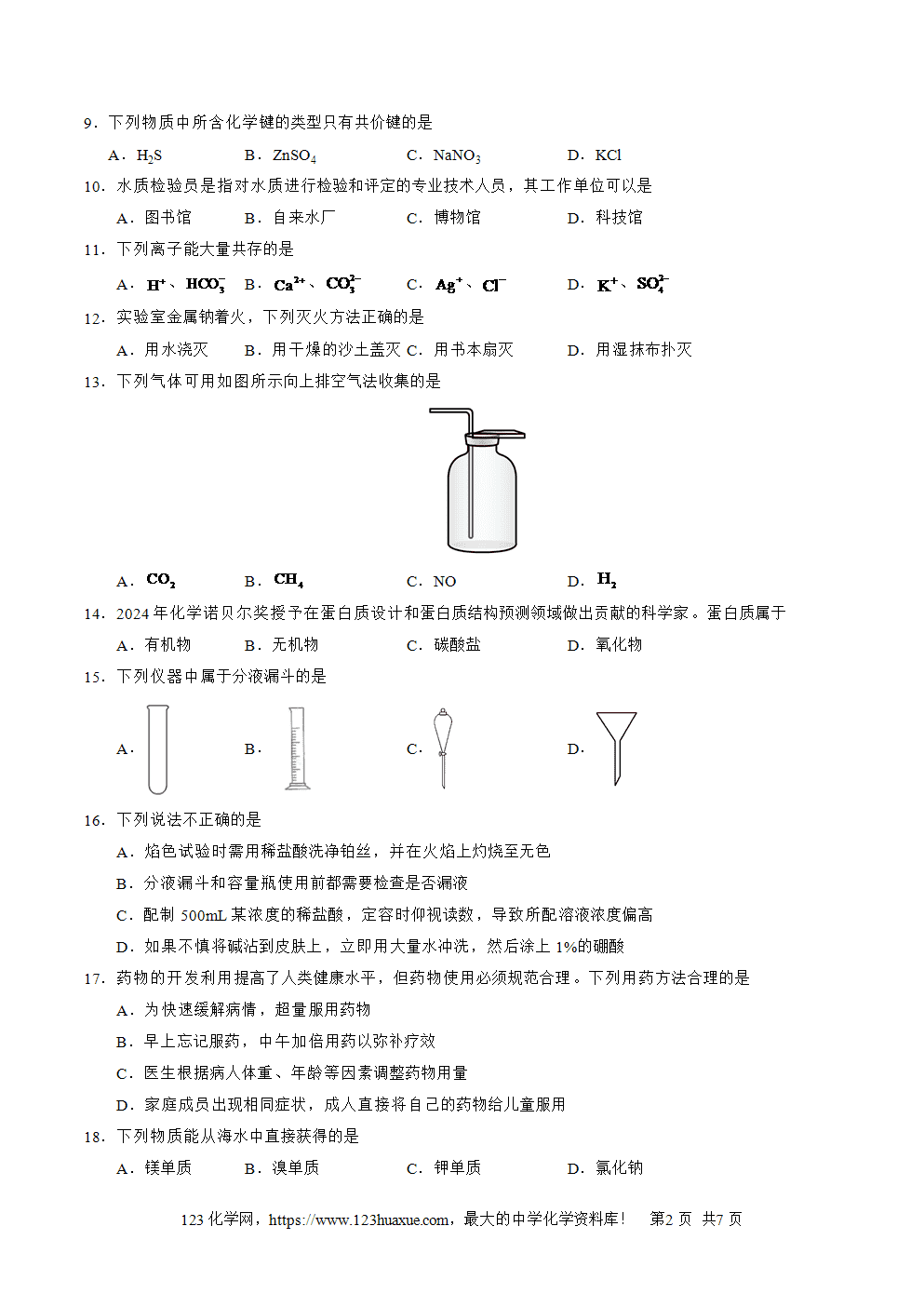
【答案】C
【分析】中子数=质量数-质子数,的质量数为17,质子数为8,中子数为9。
【详解】A.的中子数为9,A错误;
B.的中子数为9,B错误;
C.的中子数为9,C正确;
D.的中子数为9,D错误;
故选C。
3.下列属于短周期元素的是
A.Mn B.P C.Ag D.I
【答案】B
【详解】短周期元素是指第一至第三周期的前18种元素包括H、He、Li、Be、B、C、N、O、F、Ne、Na、Mg、Al、Si、P、S、Cl、Ar,只有P属于短周期元素,故选:B。
4.高铁酸钾(K2FeO4)是一种新型绿色消毒剂。高铁酸钾中铁元素的化合价是
A.+2 B.+3 C.+5 D.+6
【答案】D
【详解】已知高铁酸钾(K2FeO4)中K为+1价,O为-2价,设Fe的化合价为x价,根据化学式化合价的代数和为0可得:2×1+x+4×(-2)=0,解得:x=+6,故答案为:D。
5.下列元素的原子半径最大的是
A.C B.Na C.Al D.S
【答案】B
【详解】同主族元素原子半径从上到下随原子序数递增而增大,同周期元素原子半径从左到右随原子序数递增而减小,又锂和碳同周期,碳原子序数大于锂,则原子半径锂大于碳;锂和钠同主族且钠的原子序数大于锂,即钠的原子半径大于锂;钠、镁、铝同周期且原子序数递增,则原子半径递减,综上,原子半径最大的是钠原子,故选B。
6.下列属于电解质的是
A.氢氧化钠 B.碘酒 C.金属铝 D.饱和食盐水
【答案】A
【详解】A.氢氧化钠在水溶液里能电离出自由移动的阴阳离子导致溶液导电,所以氢氧化钠是电解质,A正确;
B.碘酒为溶液属于混合物,所以既不是电解质也不是非电解质,B错误;
C.铝是单质,所以既不是电解质也不是非电解质,C错误;
D.饱和食盐水中含有氯化钠和水是混合物,所以既不是电解质也不是非电解质,D错误;
故选A。
7.2023年诺贝尔化学奖授予了“量子点”研究的科学家。量子点材料一般是,若将其分散在适当的分散剂中所形成的分散系是
A.悬浊液 B.乳浊液 C.胶体 D.溶液
【答案】C
【详解】“量子点”的直径通常在之间,即分散质粒子直径介于1-100nm的分散系为胶体;
故选C。