提示:多个视频只播放第一个文件,完整视频请下载后播放。
教学目标
1、了解核外电子是分层排布的,了解典型元素原子核外电子的排布特点
2、了解原子结构示意图的含义及原子最外层电子数与原子化学性质的关系
3、以氯化钠为例,了解离子形成的过程,知道离子是构成物质的一种粒子
4、通过想象原子核外电子的排布,培养学生的空间想象能力
2学情分析
学生前面已经学习了分子、原子的概念,初步探索了物质构成的奥秘。原子的构成已经是学生对微观世界的第二次接触。本课题主要是在学生学习分子、原子的概念的基础上深入探究原子的内部构成及离子
3重点难点
1、原子核外电子的排布规律
2、最外层电子的结构特点
3、离子的形成
4教学过程
4.1 第一学时
4.1.1教学活动
活动1【导入】原子的结构
复习:1、原子是怎样构成的?
2、原子显电性吗? 为什么?
活动2【讲授】二、原子核外电子的排布
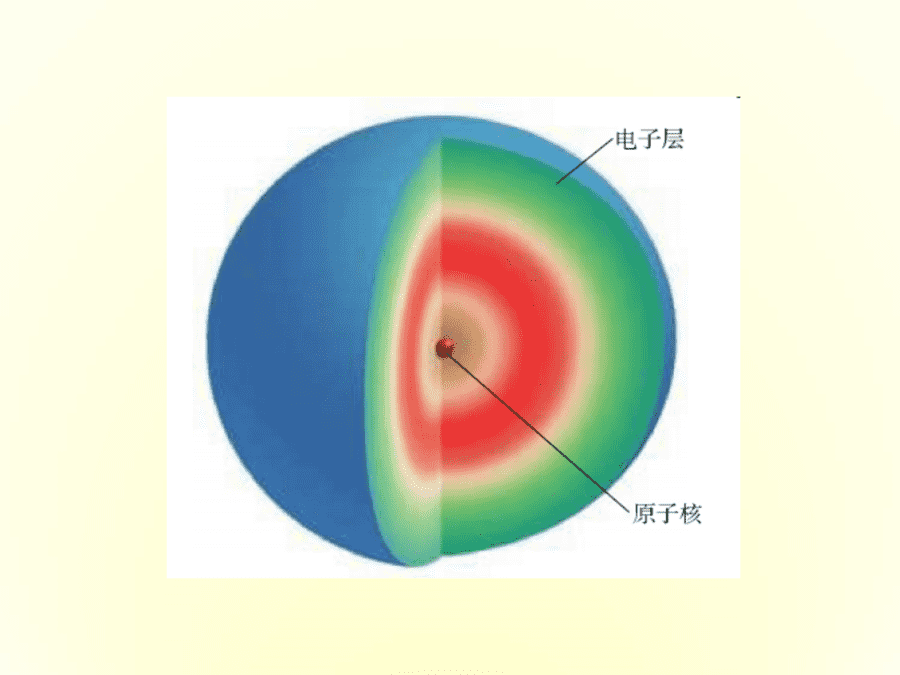
与原子相比,原子核体积更小,原子核外有很大的空间,电子就在这个空间里作高速运动。
学生:想象原子内部结构,电子如何运动
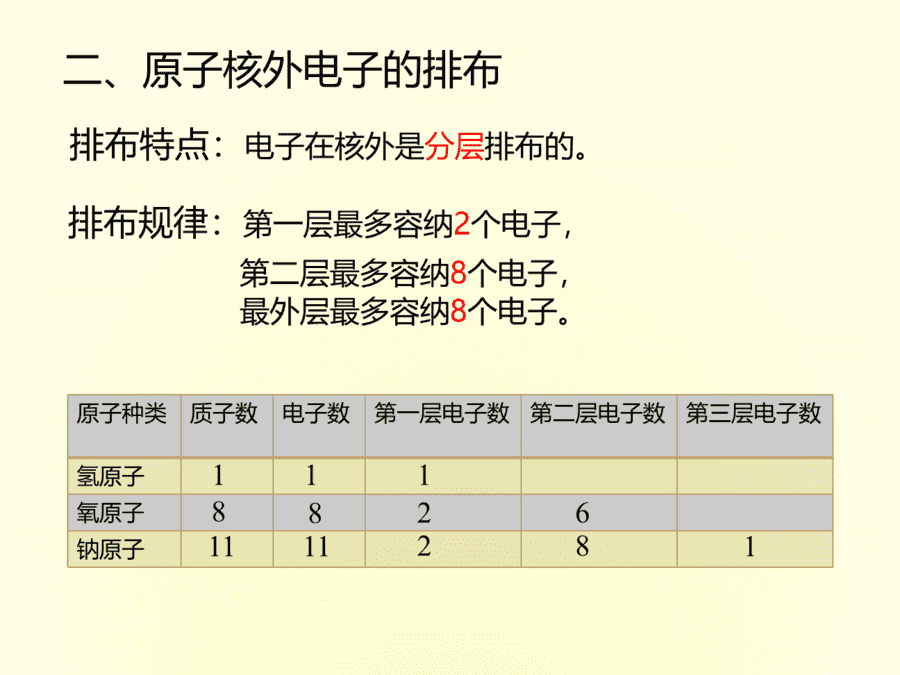
二、原子核外电子的排布
1、特点:分层排布1-7层(能量由低到高)
2、排布规则:1)第一层最多容纳2个电子
2)第二层最多容纳8个电子
3)最外层最多容纳8个电子(氦为2 )
活动3【活动】二、原子核外电子的排布
结合课本53页表3-1完成幻灯片的表格
活动4【讲授】3、原子结构示意图
如何简明、方便直观的表示原子的结构——原子结构示意图
1)画法及意义
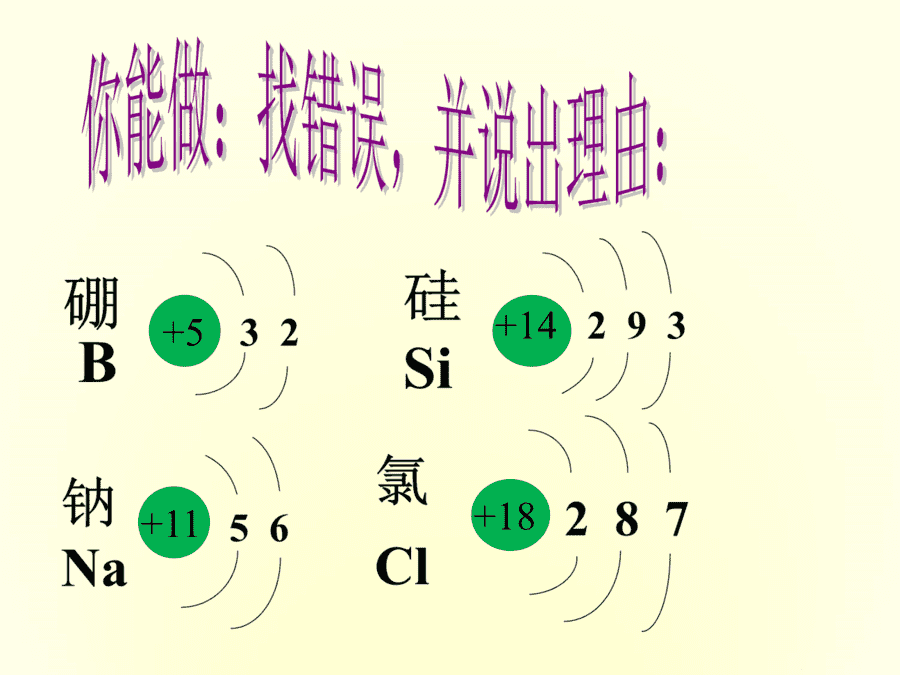
活动5【练习】二、原子核外电子的排布
画出1-18号原子的原子结构示意图
活动6【活动】二、原子核外电子的排布
总结:1)稀有气体原子最外层电子数一般为8(氦为2)
2)金属原子最外层电子数一般少于4个,易失电子
3)非金属原子最外层电子数一般多于4个,易得电子
原子的化学性质与原子最外层电子数密切相关
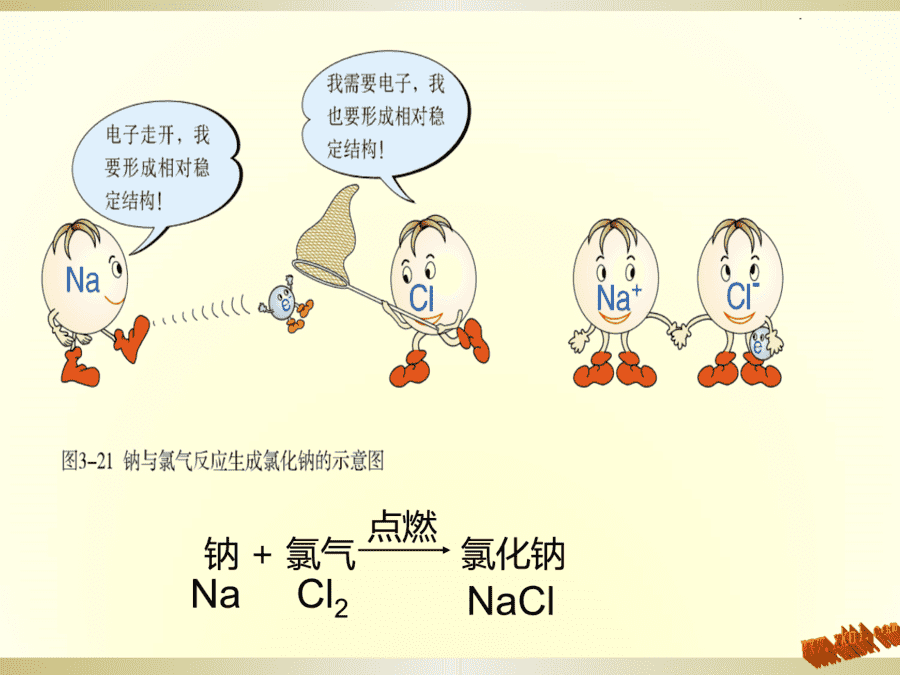
活动7【讲授】4、离子