
第12讲 氧化还原反应的概念及规律
【复习目标】
1.了解氧化还原反应的基本概念。
2.了解氧化还原反应的本质,知道常见的氧化剂和还原剂。
3.理解氧化还原反应的基本规律,了解氧化还原反应在生产、生活中的应用。
4.掌握氧化还原反应方程式的配平。
5.掌握氧化还原反应方程式的计算。
【知识精讲】
考点一 氧化还原反应的基本概念
1.氧化还原反应
(1)本质和特征
(2)氧化还原反应与四种基本反应类型间的关系
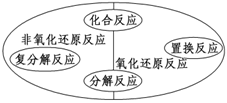
注意:有单质参加或生成的化学反应,不一定是氧化还原反应,如3O2=====放电2O3。
2.相关概念
概括为“升失氧、降得还,剂性一致、其他相反”。
对于反应C+2H2SO4(浓) 2SO2↑+CO2↑+2H2O
(1)氧化剂是浓硫酸,发生还原反应,被还原,生成还原产物SO2。
(2)还原剂是C,发生氧化反应,被氧化,生成氧化产物CO2。
(3)C和浓硫酸在反应中分别表现还原性和氧化性。
(4)反应生成1 mol CO2,浓硫酸得4mol电子,C失去4mol电子,
资料标签: