
备战2023年高考化学【一轮·夯实基础】复习精讲精练
第42讲 难溶电解质的溶解平衡
【复习目标】
1.能认识难溶电解质在水溶液中存在溶解平衡。
2.理解溶度积(Ksp)的含义,能进行相关的计算。
3.能综合运用沉淀的生成和转化原理,分析和解决生产、生活中相关的实际问题。
【知识精讲】
考点一 沉淀溶解平衡及应用
1.沉淀溶解平衡
(1)溶解平衡的含义
在一定温度下的水溶液中,当沉淀和溶解的速率相等时,即建立了沉淀溶解平衡状态。
(2)溶解平衡的建立
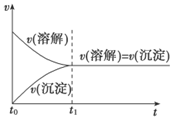
2.溶解平衡的影响因素
(1)内因:难溶电解质本身的性质,这是决定因素。
①绝对不溶的电解质是没有的。
②同是难溶电解质,溶解度差别也很大。
③易溶电解质作溶质时只要是饱和溶液也可存在溶解平衡。
(2)外因
①浓度:加水稀释,平衡向沉淀溶解的方向移动。
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动[特例Ca(OH)2]。
③同离子效应:向平衡体系中加入难溶物溶解产生的离子,平衡向生成沉淀的方向移动。
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向沉淀溶解的方向移动。
⑤加入难溶物本身:平衡不移动。
资料标签: