
1.某学习小组用“间接碘量法”测定某CuCl2晶体试样的纯度,试样不含其他能与I-发生反应的氧化性杂质,已知:2Cu2++4I-===2CuI↓+I2,I2+2S2O===S4O+2I-。取m g试样溶于水,加入过量KI固体,充分反应,用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,部分实验仪器和读数如图所示。下列说法正确的是( )
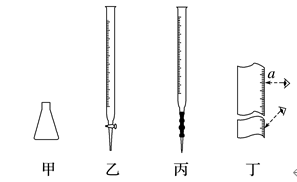
A.试样在容量瓶中溶解,滴定管选乙
B.选用淀粉作指示剂,当甲中溶液由无色变为蓝色时,即达到滴定终点
C.丁图中,滴定前滴定管的读数为(a-0.50) mL
D.对装有标准液的滴定管读数时,滴定前后读数方式如丁图所示,则测得的结果偏小
答案 D
解析 容量瓶不能作为溶解或稀释的仪器,Na2S2O3溶液显碱性,故滴定管选丙,A错误;选用淀粉作指示剂,当甲中溶液由蓝色变为无色,且半分钟内不恢复蓝色时,即达到滴定终点,B错误;滴定管的“0”刻度在上面,越往下刻度越大,故丁图中,滴定前滴定管的读数为(a+0.50) mL,C错误;对装有标准液的滴定管读数时,滴定前后读数方式如丁图所示,则读数偏小,故测得的结果偏小,D正确。
资料标签: