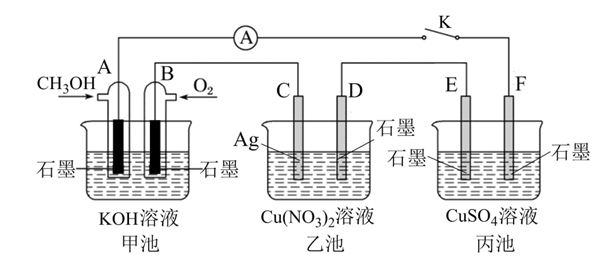
1.如图所示,若电解5 min时,测得铜电极的质量增加2.16 g。试回答:![]()
(1)电源中X极是___________(填“正”或“负”)极。
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO4)=___________mol·L-1。
(3)若A中KCl溶液的体积也是200 mL,则电解后溶液的c(OH-)=___________mol·L-1。
【答案】
(1)负
(2)0.025
(3)0.1
【分析】
铜电极的质量增加2.16 g,则铜电极是阴极,电极反应式是 ,电解5 min时,电路中转移电子的物质的量是 。
(1) 铜电极的质量增加2.16 g,说明铜电极是阴极,则X为负极;
(2) B中阳极反应式是 ,通电5 min时,生成氧气的物质的量是0.02mol÷4=0.005mol, 则B中阴极生成氢气的物质的量是 ,生成氢气转移电子0.01mol,根据电子守恒,生成铜转移电子0.02mol-0.01mol=0.01mol,生成铜的物质的量是 ,溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO4)= ;
(3) A中电解的总反应式是 ↑+H2↑ ,电解5 min时,电路中转移电子的物质的量是0.02mol,则A中生成KOH的物质的量是0.02mol,若A中KCl溶液的体积也是200 mL,则电解后溶液的c(OH-)= 。
【提分秘籍】
根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
【变式演练】
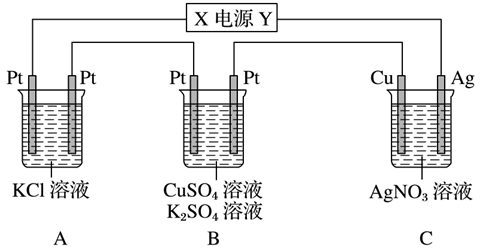
1.某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量,体积均为1L),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题: