[复习目标] 1.掌握速率、平衡图像的分析方法及类型。2.掌握实际工业生产中的陌生图像的分析方法。
1.(2022·全国甲卷,28)金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。回答下列问题:
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1 000 ℃时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)===TiCl4(g)+O2(g) ΔH1=+172 kJ·mol-1,Kp1=1.0×10-2
(ⅱ)碳氯化:TiO2(s)+2Cl2(g)+2C(s)===TiCl4(g)+2CO(g) ΔH2=-51 kJ·mol-1,Kp2=1.2×1012 Pa
①反应2C(s)+O2(g)===2CO(g)的ΔH为________ kJ·mol-1,Kp=__________Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是__________________________________。
③对于碳氯化反应:增大压强,平衡________移动(填“向左”“向右”或“不”);温度升高,平衡转化率________(填“变大”“变小”或“不变”)。
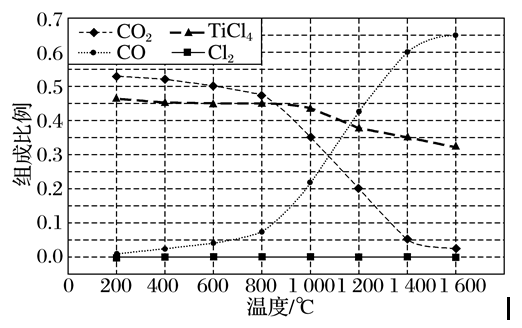
(2)在1.0×105 Pa,将TiO2、C、Cl2以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。