
化学反应速率与化学平衡归因分析
1.研究碳及其化合物的资源化利用具有重要的意义。已知下列热化学方程式:
反应Ⅰ:CO2(g)+4H2(g)CH4(g)+2H2O(g) ΔH1=-164.9 kJ·mol-1
反应Ⅱ:CO2(g)+H2(g)CO(g)+H2O(g) ΔH2=+41.2 kJ·mol-1
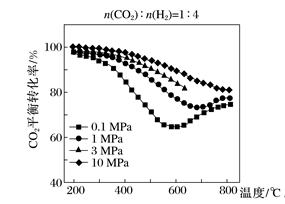
将n(CO2)∶n(H2)=1∶4的混合气体充入密闭容器中发生上述反应Ⅰ、Ⅱ,在不同温度和压强时,CO2的平衡转化率如图。0.1 MPa时,CO2的转化率在600 ℃之后,随温度升高而增大的主要原因是____
资料标签: