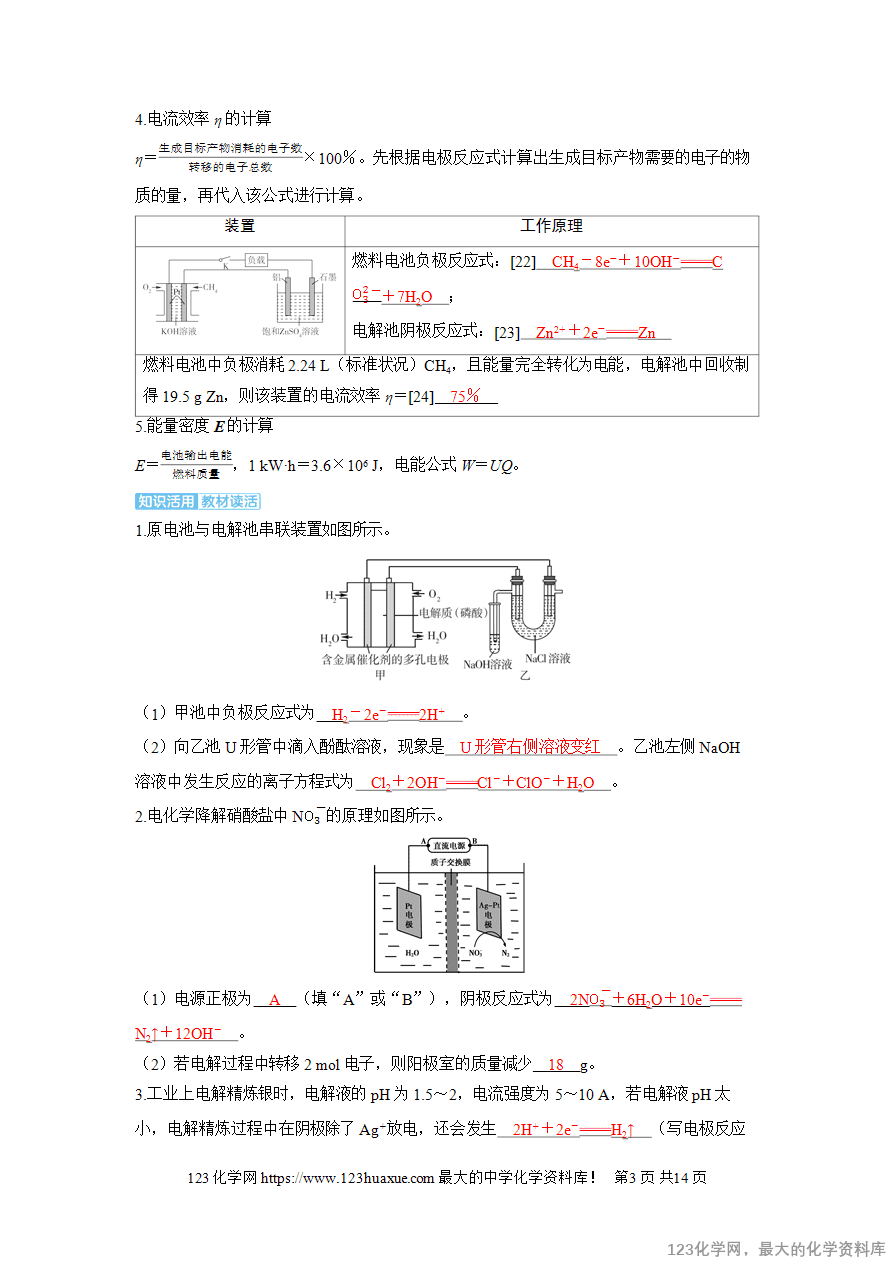
原电池与电解池串联装置如图所示。
(1)甲池中负极反应式为 H2-2e-2H+ 。
(2)向乙池U形管中滴入酚酞溶液,现象是 U形管右侧溶液变红 。乙池左侧NaOH溶液中发生反应的离子方程式为 Cl2+2OH-Cl-+ClO-+H2O 。
2.电化学降解硝酸盐中N的原理如图所示。
(1)电源正极为 A (填“A”或“B”),阴极反应式为 2N+6H2O+10e-N2↑+12OH- 。
(2)若电解过程中转移2 mol电子,则阳极室的质量减少 18 g。
3.工业上电解精炼银时,电解液的pH为1.5~2,电流强度为5~10 A,若电解液pH太小,电解精炼过程中在阴极除了Ag+放电,还会发生 2H++2e-H2↑ (写电极反应式),若用10 A的电流电解60 min 后,得到32.4 g Ag,则该电解池的电解效率为 80.4 %。(保留小数点后一位;通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率;法拉第常数为 96 500 C·mol-1 )
4.二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度高于甲醇直接燃料电池(5.93 kW·h·kg-1)。若电解质为酸性,二甲醚直接燃料电池的负极反应为 CH3OCH3+3H2O-12e-2CO2↑+12H+ ,1 mol二甲醚分子经过电化学氧化,可以产生 12 mol电子的电量;该电池的理论输出电压为1.20 V,能量密度E= ≈8.39 kW·h·kg-1 (列式计算,能量密度=电池输出电能/燃料质量,1 kW·h=3.6×106 J,F=96 500 C·mol-1)。