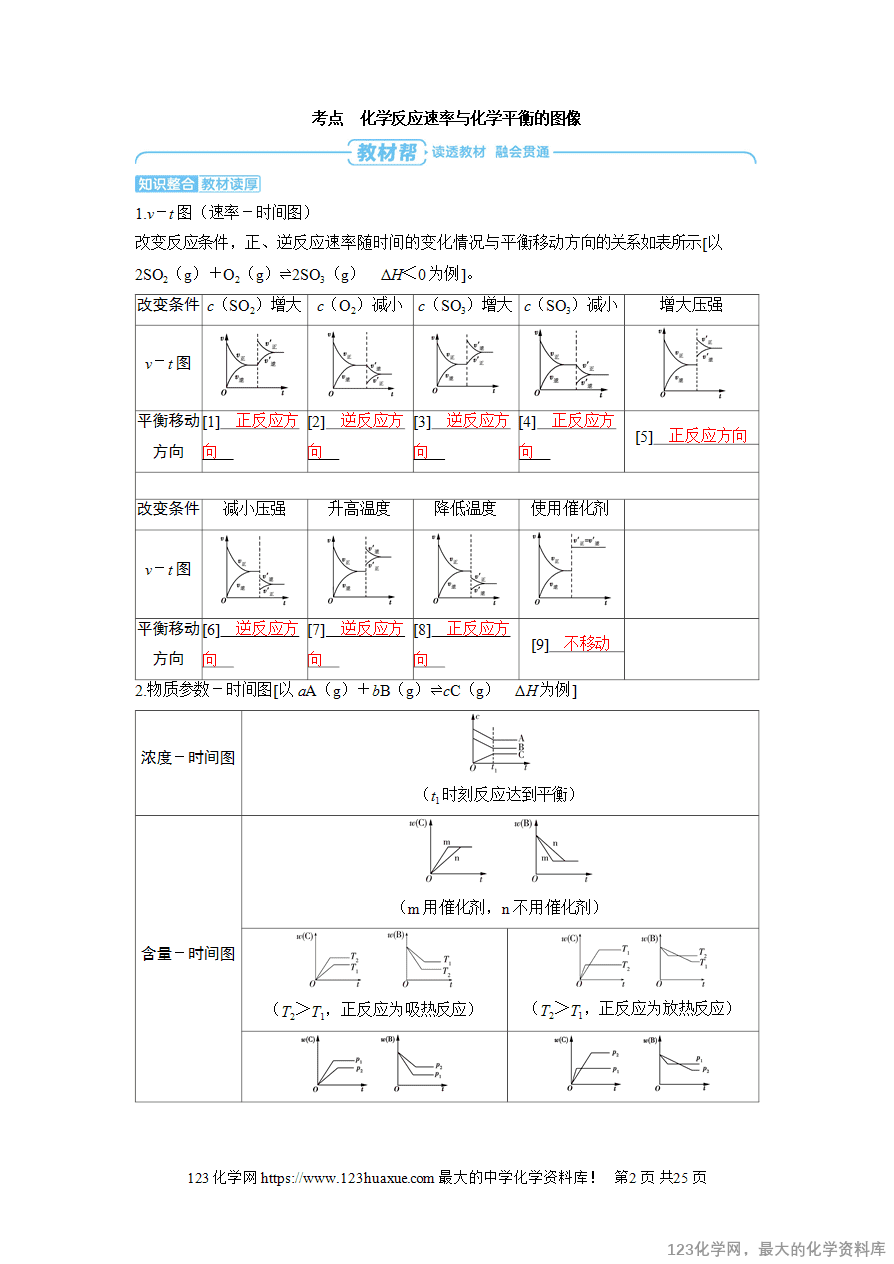
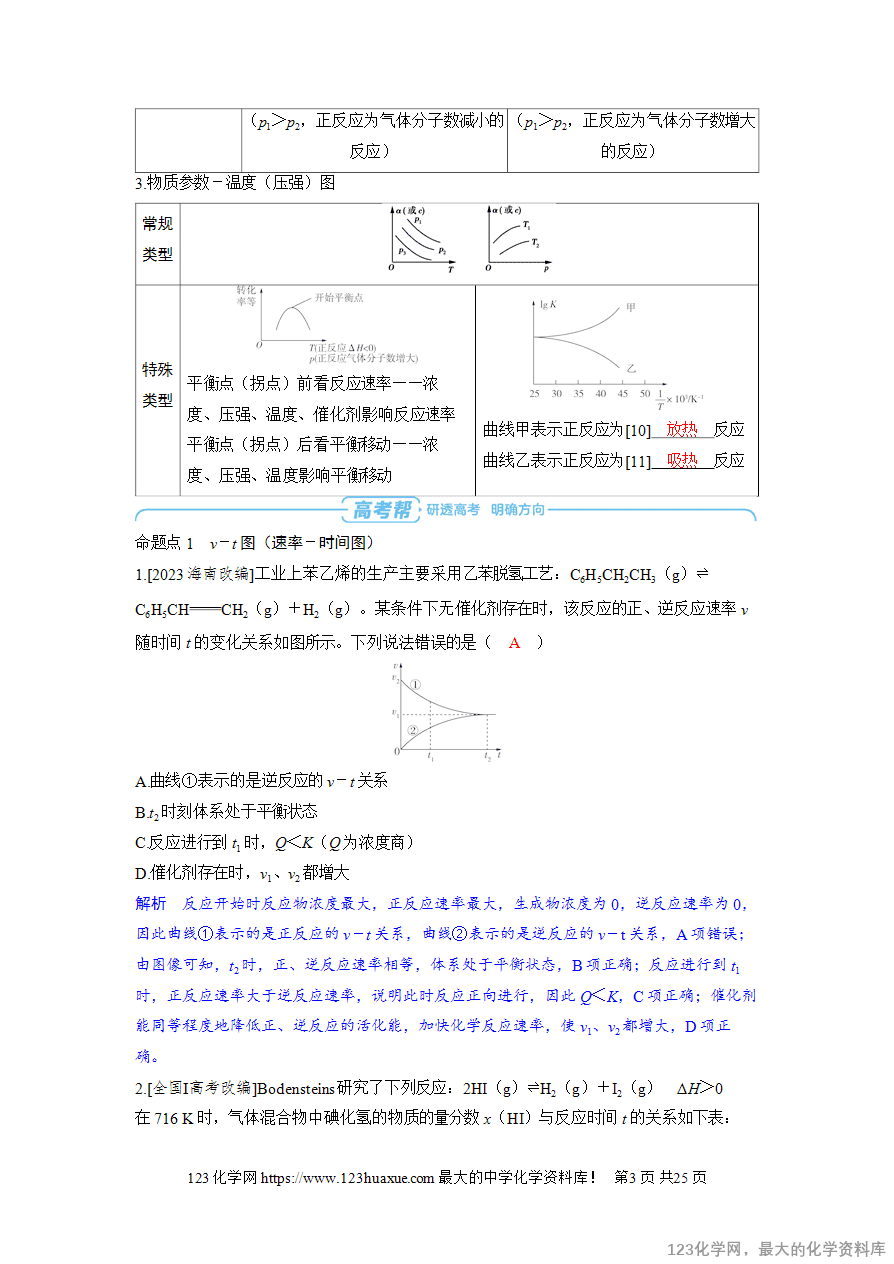
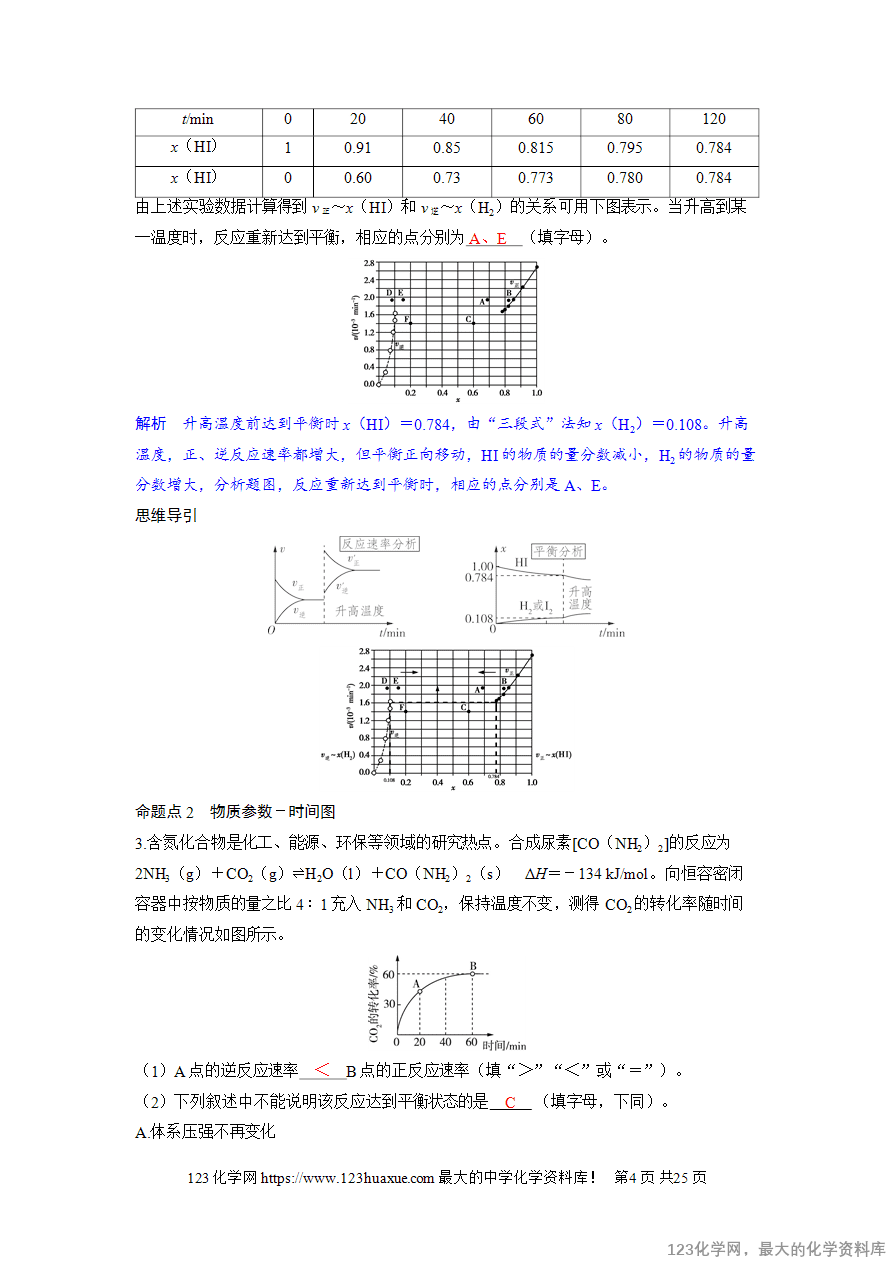
命题点1 v-t图(速率-时间图)
1.[2023海南改编]工业上苯乙烯的生产主要采用乙苯脱氢工艺:C6H5CH2CH3(g) C6H5CHCH2(g)+H2(g)。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法错误的是( A )
A.曲线①表示的是逆反应的v-t关系
B.t2时刻体系处于平衡状态
C.反应进行到t1时,Q<K(Q为浓度商)
D.催化剂存在时,v1、v2都增大
解析 反应开始时反应物浓度最大,正反应速率最大,生成物浓度为0,逆反应速率为0,因此曲线①表示的是正反应的v-t关系,曲线②表示的是逆反应的v-t关系,A项错误;由图像可知,t2时,正、逆反应速率相等,体系处于平衡状态,B项正确;反应进行到t1时,正反应速率大于逆反应速率,说明此时反应正向进行,因此Q<K,C项正确;催化剂能同等程度地降低正、逆反应的活化能,加快化学反应速率,使v1、v2都增大,D项正确。
2.[全国Ⅰ高考改编]Bodensteins研究了下列反应:2HI(g)H2(g)+I2(g) ΔH>0
在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为 A、E (填字母)。
解析 升高温度前达到平衡时x(HI)=0.784,由“三段式”法知 x(H2)=0.108。升高温度,正、逆反应速率都增大,但平衡正向移动,HI的物质的量分数减小,H2的物质的量分数增大,分析题图,反应重新达到平衡时,相应的点分别是A、E。