填空题
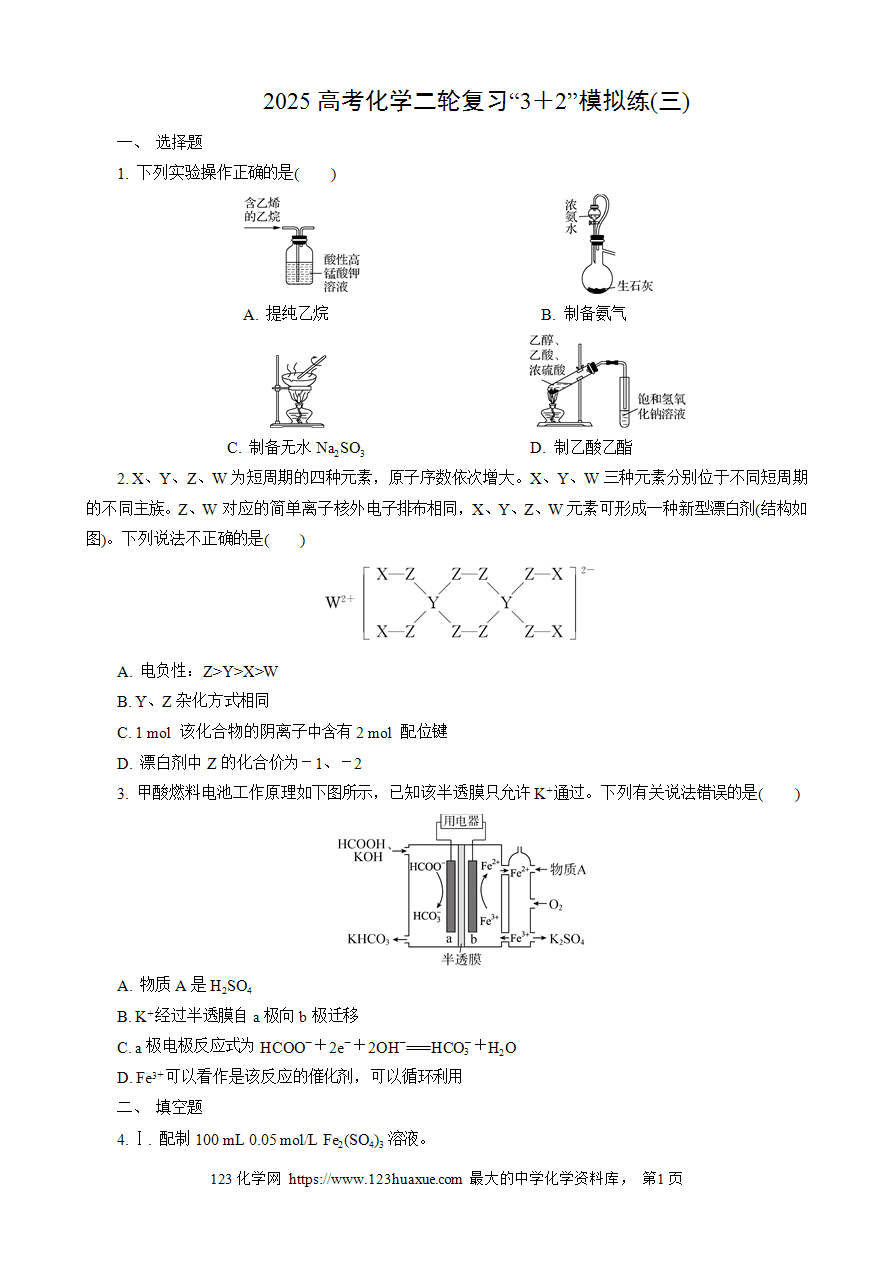
4. Ⅰ. 配制100 mL 0.05 mol/L Fe2(SO4)3溶液。
(1)该实验需要用到的玻璃仪器有:烧杯、量筒、玻璃棒、____________、______________________。
(2)为了防止Fe2(SO4)3水解,在配置过程中可以加入少量__________。
Ⅱ.探究Fe2(SO4)3与Cu的反应。
[原理预测] (3)请写出Fe2(SO4)3与Cu的反应的离子方程式:__________________________ ____________________。
[开展实验] 某实验小组在进行Fe2(SO4)3与Cu的反应时观察到了异常现象,决定对其进行进一步的探究。
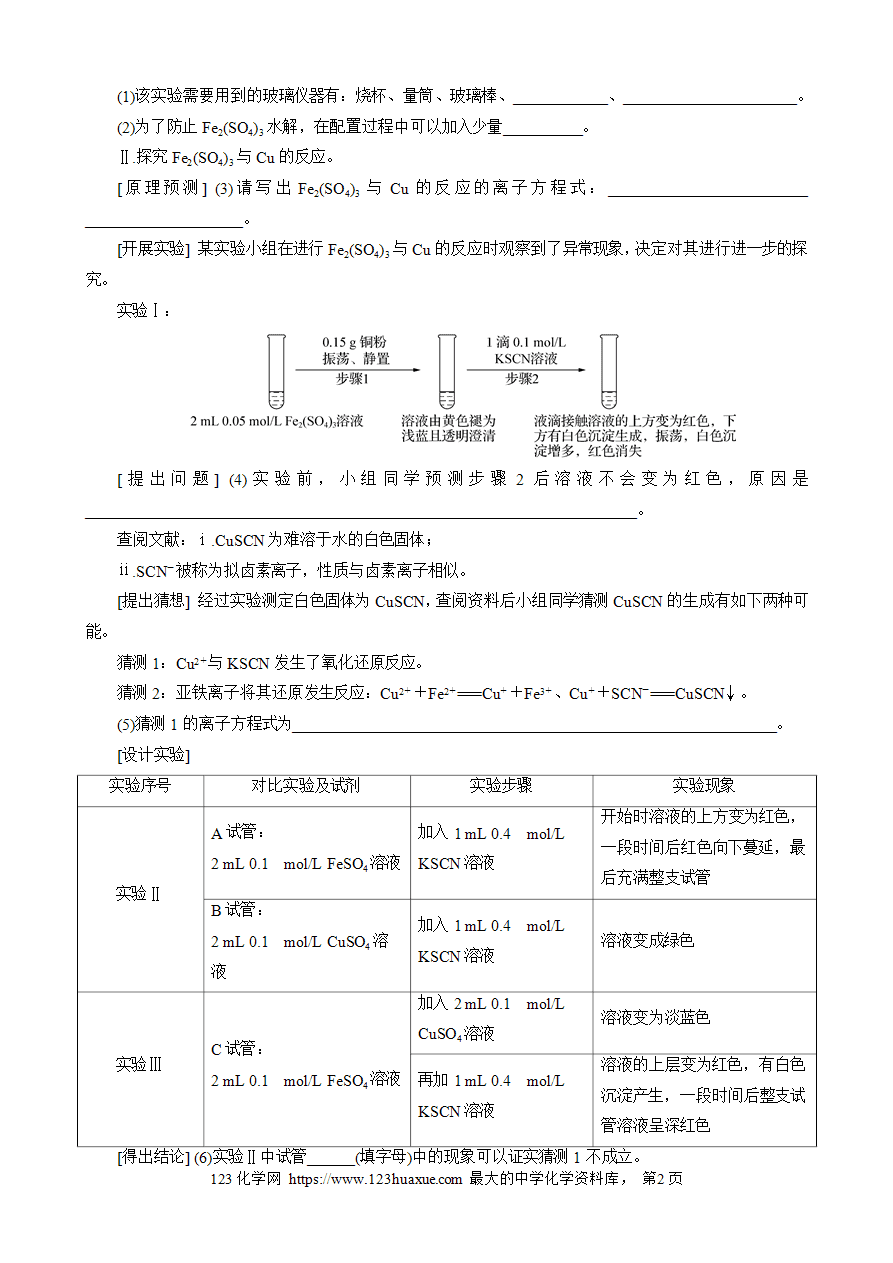
实验Ⅰ:
[提出问题] (4)实验前,小组同学预测步骤2后溶液不会变为红色,原因是______________________________________________________________________。
查阅文献:ⅰ.CuSCN为难溶于水的白色固体;
ⅱ.SCN-被称为拟卤素离子,性质与卤素离子相似。
[提出猜想] 经过实验测定白色固体为CuSCN,查阅资料后小组同学猜测CuSCN的生成有如下两种可能。
猜测1:Cu2+与KSCN发生了氧化还原反应。
猜测2:亚铁离子将其还原发生反应:Cu2++Fe2+===Cu++Fe3+、Cu++SCN-===CuSCN↓。
(5)猜测1的离子方程式为____________________________________