






(1)知道原子的结构及构成原子的微粒间的关系;根据原子核外电子的排布规律,能画出1~20号元素的原子结构示意图。
(2)了解预测、假设、模型等方法在科学家研究原子结构中的作用。
【内容分析】
本节内容是原子结构。关于原子结构,以初中已有知识为基础,教材通过“思考与讨论”,引导学生观察稀有气体元素原子核外电子排布,发现规律,从而归纳出1~20号元素的原子核外电子排布。这样的呈现方式,重在启发学生思考,培养逻辑思维能力。第一章“方法导引”介绍了科学方法一模型,而本节呈现的科学史话----原子结构模型的演变,有利于学生进一步理解科学模型的含义。对于该内容有两种处理方法,第一,让学生自主阅读,学生阅读后,可以了解人类对原子结构的认识逐步深人的过程,能够体会到现在学习的科学理论只代表人类对客观事物认识的一个阶段,而人们对客观事物的认识,还会不断深人和发展。第二,教师查阅资料,整理成线索,让学生通过图片等,对于原子结构的发展形成更直观的认识。本节课采用的是第二种处理方式。
【教学重点和难点】
重点:原子核外电子排布的规律
【教学流程】
【学习任务一】回顾历史,掌握模型构建的学习方法
古人关于万物构成的思考:惠施(战国)的十个命题,主要是对自然界的分析,其中有些含有辩证的因素。他说:“至大无外,谓之大一;至小无内,谓之小一。”“大一”是说整个空间大到无所不包,不再有外部;“小一”是说物质最小的单位,小到不可再分割,不再有内部。
古希腊哲学家德谟克利特(Democritus,约公元前460—公元前370)曾经指出,物质是由不可分割的微粒(也称为“原子”)构成的。
【思考】原子真的是不可分割的球体吗?
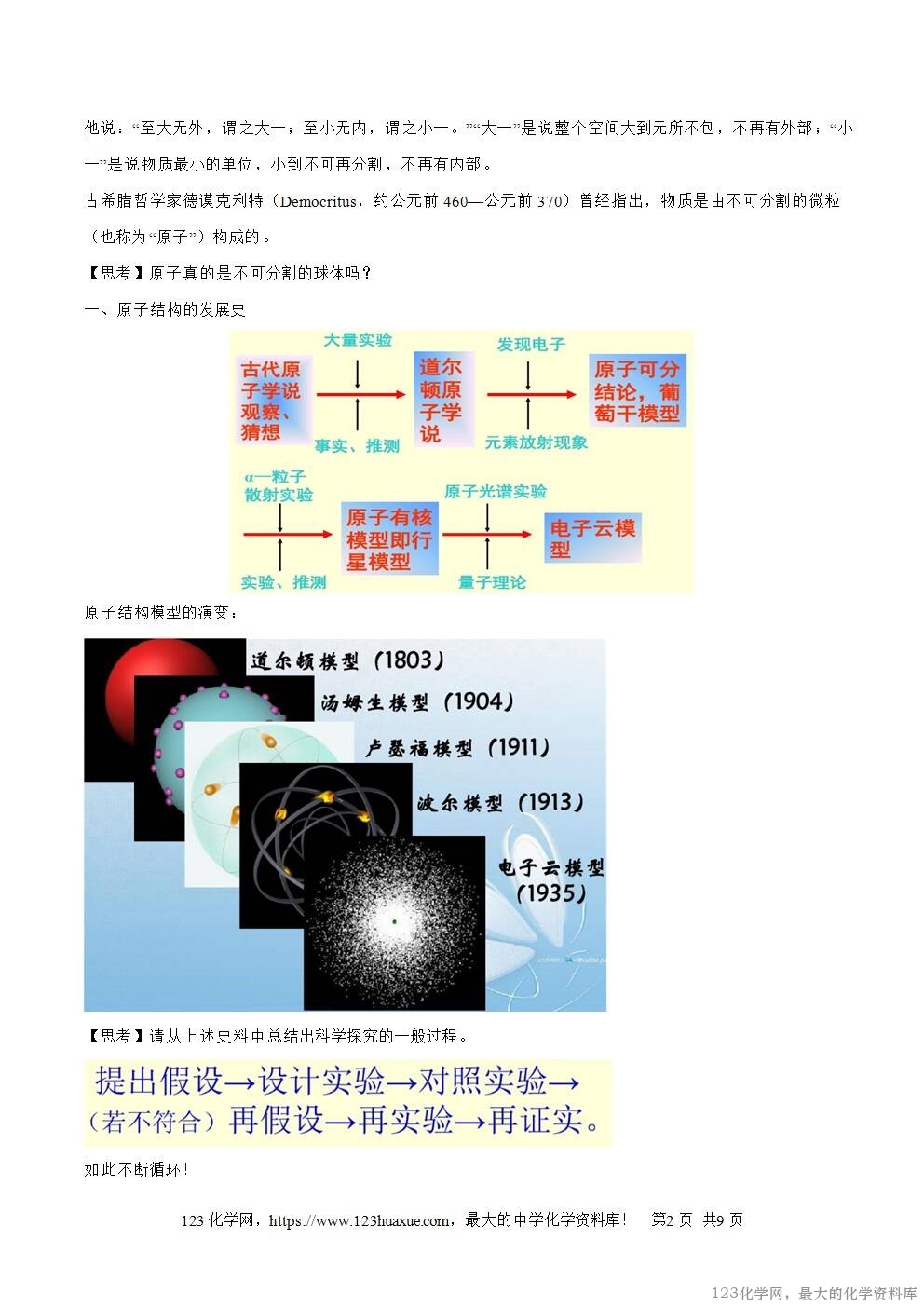
一、原子结构的发展史
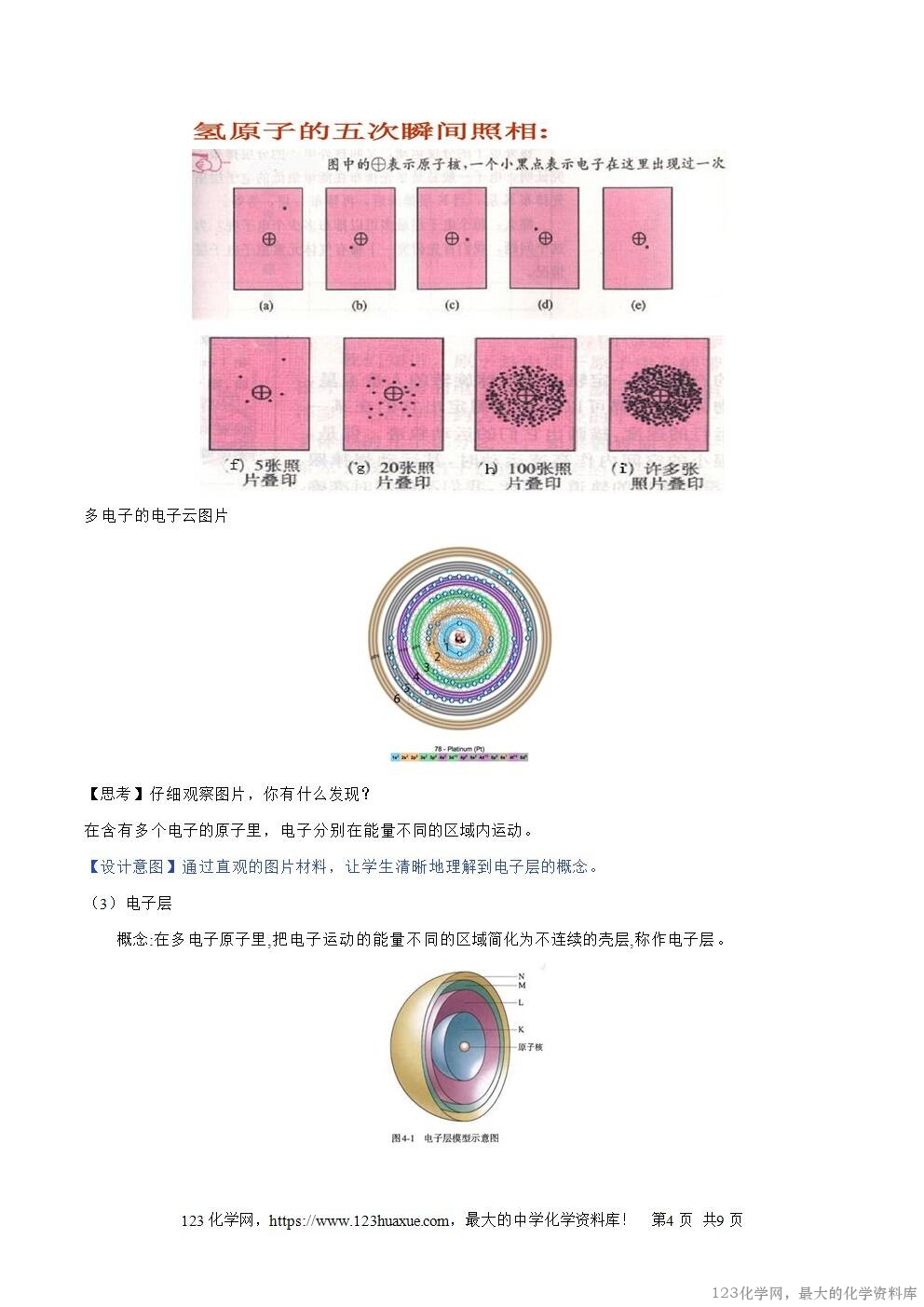
原子结构模型的演变:
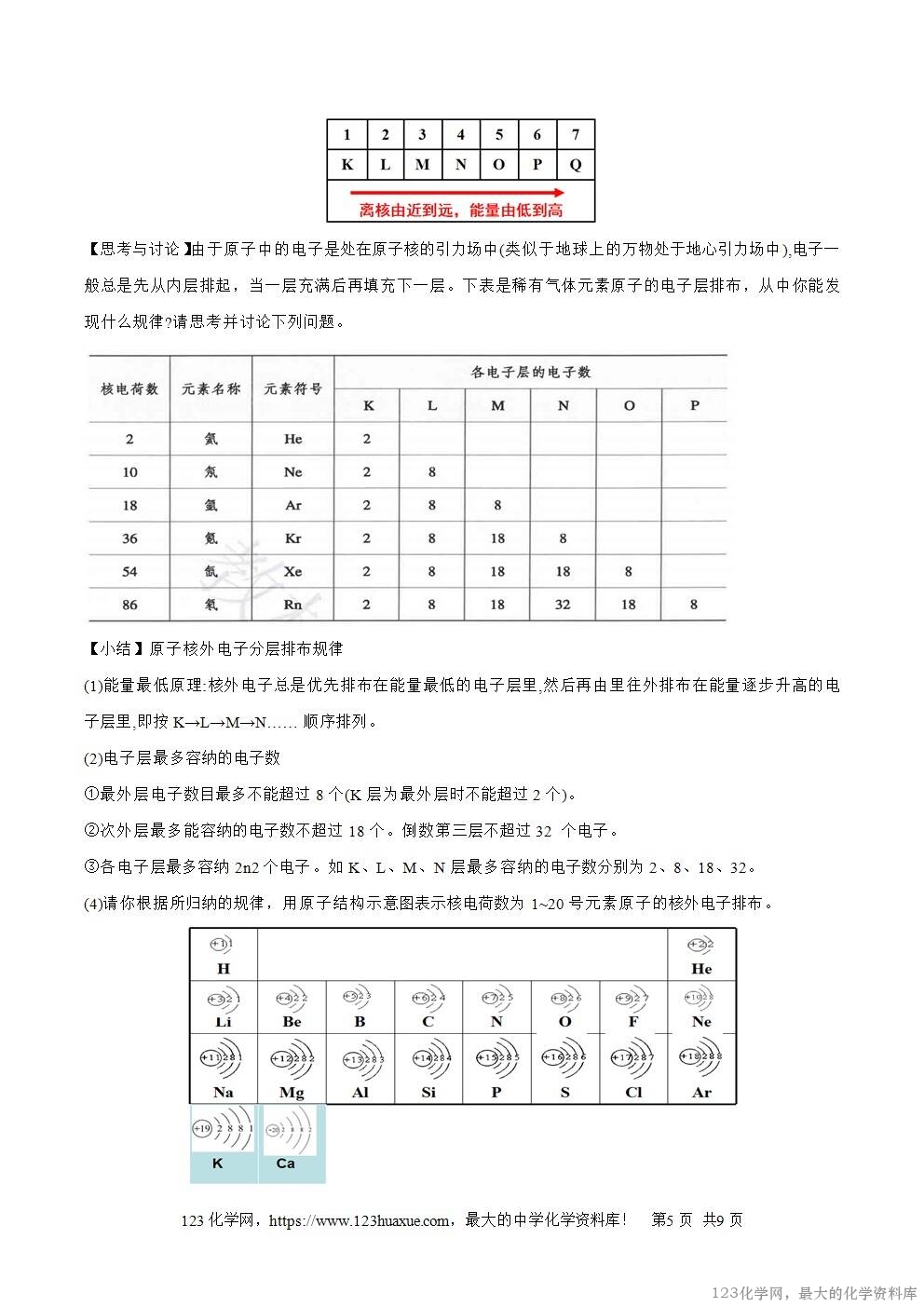
【思考】请从上述史料中总结出科学探究的一般过程。
如此不断循环!
【设计意图】通过原子结构的发展史,以及原子结构模型的演变,可以让学生更直观地了解原子结构的真实情况,并让学生体会到现在学习的科学理论只代表人类对客观事物认识的一个阶段,而人们对客观事物的认识,还会不断深人和发展。
二、原子结构
(2)质量数:质子和中子的相对质量都近似为1,忽略电子的质量,将原子核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数。
质量数(A)=质子数(Z)+中子数(N)
【评价任务一】
判断下列说法是否正确
(1)原子呈电中性是因为中子不带电( )
(2)质子数和中子数决定原子的质量( )
(3)原子的质量数就是原子的相对原子质量( )
(4)微粒中的质子数与核外电子数一定相等( )
(5)某种氯原子的中子数是18,则其质量数是35,核外电子数是17( )
【答案】× √ × × √
【设计意图】即时检测学生的学习成果,为“位构性”的学习打下基础。
【学习任务二】理论探究,掌握原子结构
【思考】原子核外电子是如何运动的?
高速运动,接近光速;
没有确定的轨迹,不能同时准确地测定电子在某一时刻所处的位置和运动速度,也不能描绘出它的运动轨迹。
如何描述核外电子的运动?
只能用统计的观点指出它在原子核外空间某处出现机会的多少。
用“电子云”形象地描述核外电子的运动。
多电子的电子云图片