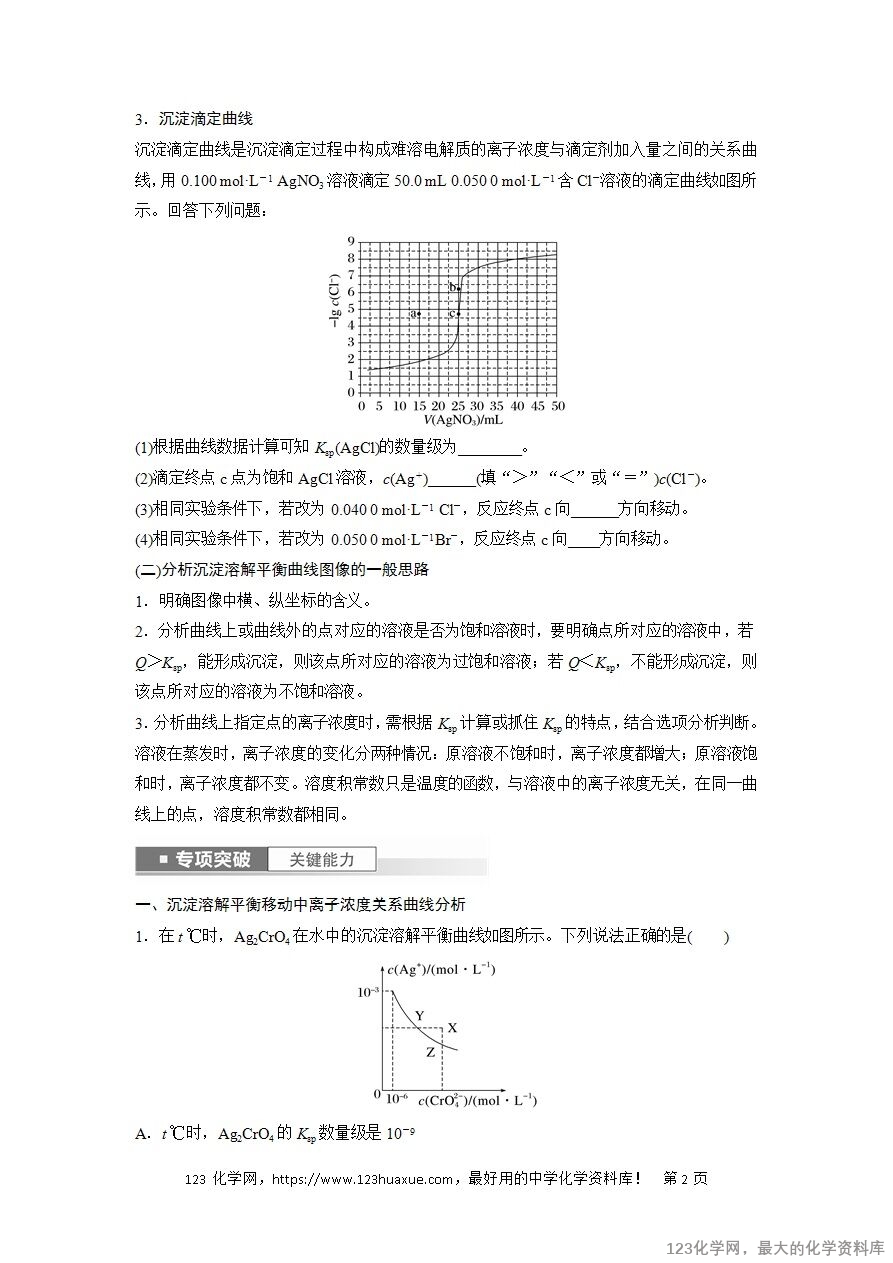
沉淀滴定曲线
沉淀滴定曲线是沉淀滴定过程中构成难溶电解质的离子浓度与滴定剂加入量之间的关系曲线,用0.100 mol·L-1 AgNO3溶液滴定50.0 mL 0.050 0 mol·L-1含Cl-溶液的滴定曲线如图所示。回答下列问题:
(1)根据曲线数据计算可知Ksp(AgCl)的数量级为________。
(2)滴定终点c点为饱和AgCl溶液,c(Ag+)______(填“>”“<”或“=”)c(Cl-)。
(3)相同实验条件下,若改为0.040 0 mol·L-1 Cl-,反应终点c向______方向移动。
(4)相同实验条件下,若改为0.050 0 mol·L-1Br-,反应终点c向____方向移动。
(二)分析沉淀溶解平衡曲线图像的一般思路
1.明确图像中横、纵坐标的含义。
2.分析曲线上或曲线外的点对应的溶液是否为饱和溶液时,要明确点所对应的溶液中,若Q>Ksp,能形成沉淀,则该点所对应的溶液为过饱和溶液;若Q<Ksp,不能形成沉淀,则该点所对应的溶液为不饱和溶液。
3.分析曲线上指定点的离子浓度时,需根据Ksp计算或抓住Ksp的特点,结合选项分析判断。溶液在蒸发时,离子浓度的变化分两种情况:原溶液不饱和时,离子浓度都增大;原溶液饱和时,离子浓度都不变。溶度积常数只是温度的函数,与溶液中的离子浓度无关,在同一曲线上的点,溶度积常数都相同。