
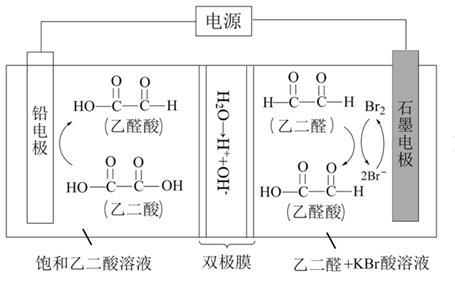
1.乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。图中的双极膜中间层中的 解离为 和 ,并在直流电场作用下分别问两极迁移。下列说法正确的是
A. 在上述电化学合成过程中只起电解质的作用
B.阳极上的反应式为: +2H++2e-= +H2O
C.制得 乙醛酸,理论上外电路中迁移了 电子
D.双极膜中间层中的 在外电场作用下向铅电极方向迁移
【答案】D
【分析】
该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳极,阳极上Br-被氧化为Br2,Br2将乙二醛氧化为乙醛酸,双极膜中间层的H+在直流电场作用下移向阴极,OH-移向阳极。
【详解】
A.KBr在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生成的Br2为乙二醛制备乙醛酸的中间产物,故A错误;
B.阳极上为Br-失去电子生成Br2,Br2将乙二醛氧化为乙醛酸,故B错误;
C.电解过程中阴阳极均生成乙醛酸,1mol乙二酸生成1mol乙醛酸转移电子为2mol,1mol乙二醛生成1mol乙醛酸转移电子为2mol,根据转移电子守恒可知每生成1mol乙醛酸转移电子为1mol,因此制得2mol乙醛酸时,理论上外电路中迁移了2mol电子,故C错误;
D.由上述分析可知,双极膜中间层的H+在外电场作用下移向阴极,即H+移向铅电极,故D正确;
综上所述,说法正确的是D项,故答案为D。
2.沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是
A.阳极发生将海水中的 氧化生成 的反应
B.管道中可以生成氧化灭杀附着生物的
C.阴极生成的 应及时通风稀释安全地排入大气
D.阳极表面形成的 等积垢需要定期清理
【答案】D
【分析】
海水中除了水,还含有大量的Na+、Cl-、Mg2+等,根据题干信息可知,装置的原理是利用惰性电极电解海水,阳极区溶液中的Cl-会优先失电子生成Cl2,阴极区H2O优先得电子生成H2和OH-,结合海水成分及电解产物分析解答。
【详解】
A.根据分析可知,阳极区海水中的Cl-会优先失去电子生成Cl2,发生氧化反应,A正确;
B.设置的装置为电解池原理,根据分析知,阳极区生成的Cl2与阴极区生成的OH-在管道中会发生反应生成NaCl、NaClO和H2O,其中NaClO具有强氧化性,可氧化灭杀附着的生物,B正确;
C.因为H2是易燃性气体,所以阴极区生成的H2需及时通风稀释,安全地排入大气,以排除安全隐患,C正确;
D.阴极的电极反应式为:2H2O+2e-=H2↑+2OH-,