
一、选择题:每小题只有一个选项符合题意。
1.如图表示铁与不同浓度硝酸反应时,各种还原产物的相对含量与硝酸溶液浓度的关系,则下列说法不正确的是( )
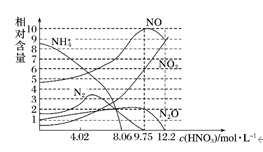
A.一般来说,硝酸与铁反应的还原产物不是单一的
B.用一定量的铁粉与大量的9.75 mol·L-1 HNO3溶液反应得到标准状况下气体2.24 L,则参加反应的硝酸的物质的量为0.1 mol
C.硝酸的浓度越大,其还原产物中价态越高的成分越多
D.当硝酸浓度为9.75 mol·L-1时还原产物是NO、NO2、N2O,且其物质的量之比为5∶3∶1
2.(湖南、江西十四校联考)向25 mL 12.0 mol·L-1浓硝酸中加入足量的铜,充分反应后共收集到标准状况下2.24 L NO和NO2的混合气体(不考虑NO2与N2O4的相互转化),则参加反应的铜的质量为( )
A.3.2 g B.6.4 g
C.12.8 g D.19.2 g
3.(太原期末)将14 g铁粉溶于1 L稀硝酸中恰好完全反应,放出标准状况下4.48 L NO气体(假设是唯一还原产物),则原溶液中硝酸的浓度为( )
A.1.0 mol·L-1 B.0.4 mol·L-1
C.0.6 mol·L-1 D.0.8 mol·L-1
4.将11.2 g的Mg—Cu混合物完全溶解于足量的硝酸中,收集反应产生的气体x(假定产生的气体全部逸出)。再向所得溶液中加入足量的NaOH溶液,产生21.4 g沉淀。根据题意推断气体x的成分可能是( )
A.0.3 mol NO2和0.3 mol NO
B.0.2 mol NO2和0.1 mol N2O4
C.0.6 mol NO
D.0.1 mol NO、0.2 mol NO2和0.05 mol N2O4
5.将Mg和Cu的合金2.64 g,投入适量的稀HNO3中恰好反应,固体全部溶解时,收集的还原产物为NO,体积为0.896 L(标准状况下),向反应后的溶液中加入2 mol·L-1NaOH溶液60 mL时,金属离子恰好完全沉