分析:
第一步:依题意,铬元素的化合价降低,故K2Cr2O7是氧化剂,Cr3+是还原产物;碳元素的化合价升高,故Na2C2O4(碳元素化合价为+3价)是还原剂,CO2是氧化产物。
第二步:按“氧化剂+还原剂——氧化产物+还原产物”把离子方程式初步写成: ,由 ,铬元素降了3价,1mol 共得到6mole-,由C2O42- CO2,碳元素升了1价,1molC2O42-共失去2mole-,故在C2O42-前配3,在氧化产物CO2前配6,在 前配1,在还原产物 前配2,即 。
第三步:反应在硫酸中进行,故在左边补充H+,右边补充H2O, +3C2O42-+H+ 2 +6CO2↑+H2O
第四步:依据电荷守恒及H、O原子守恒配平如下:
+3C2O42-+14H+ 2 +6CO2↑+7H2O
【提分秘籍】
工艺流程中的氧化还原方程式的书写方法
1.细读题干寻找提纯对象,结合工艺流程示意图分析被提纯元素的存在形式及杂质的去除情况。
2.确定未知反应的反应物和生成物,根据题意分析溶液环境,配平氧化还原方程式。
3.配平步骤:
第1步:根据题干信息或流程图,判断氧化剂、还原剂、氧化产物、还原产物。
第2步:按“氧化剂+还原剂——氧化产物+还原产物”写出方程式,根据得失电子守恒对方程式进行配平。
第3步:根据电荷守恒和反应物的酸碱性,在方程式左边或右边补充H+、OH-或H2O等。
第4步:根据质量守恒配平反应方程式。
【变式演练】
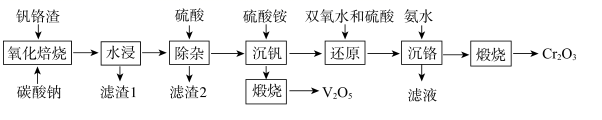
1.2020年5月课题组公布了提取钒铬的工艺流程: