第1课时 电解原理
1.实验室中用电解水的方法制取氢气和氧气,为了增强溶液的导电性最好加入下列电解质中的( B )
A.NaCl B.Na2SO4
C.CuCl2 D.AgNO3
解析:A项,加入NaCl,发生2NaCl+2H2O2NaOH+H2↑+Cl2↑,生成氯气,影响氧气的生成,错误;B项,加入Na2SO4,增大溶液浓度,导电性增强,且不影响H2和O2的生成,正确;C项,加入CuCl2,电解CuCl2溶液时一极析铜,另一极产生氯气,不是电解的水,错误;D项,加入AgNO3,在阴极上析出Ag,影响氢气的生成,错误。
2.用惰性电极电解稀H2SO4、Cu(NO3)2、NaCl的混合液,最初一段时间阴极和阳极上析出的物质分别是( B )
A.H2和Cl2 B.Cu和Cl2
C.H2和O2 D.Cu和O2
解析:由题意知,溶液中存在H+、Cu2+、Na+、SO、NO、Cl-、OH-,根据离子的放电顺序,阳离子为Cu2+>H+>Na+,阴离子为Cl->OH->SO、NO,则最初一段时间,阴极Cu2++2e-===Cu,阳极2Cl--2e-===Cl2。
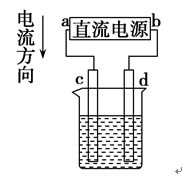
3.如图所示是电解CuCl2溶液的装置,其中c、d为石墨电极。