
微题型62 金属的腐蚀和防护
1.下列叙述正确的是( )
A.原电池的负极发生还原反应
B.电化学腐蚀的实质是金属单质失去电子形成阳离子,而电子直接转移给氧化剂
C.金属在中性环境中主要发生析氢腐蚀
D.钢铁在潮湿环境中锈蚀时,开始生成Fe(OH)2,而后逐渐变成Fe(OH)3和Fe2O3·xH2O
答案 D
解析 原电池的负极发生失电子的氧化反应,故A错误;金属的电化学腐蚀实质是M-ne-===Mn+,是金属失电子形成阳离子,而电子通过外电路形成电流,再转移给氧化剂的过程,故B错误;金属在酸性环境中,发生析氢腐蚀,在中性环境下主要发生吸氧腐蚀,故C错误;钢铁在潮湿环境中主要发生吸氧腐蚀,负极上是铁放电生成Fe2+,即Fe-2e-===Fe2+,正极上氧气放电,即O2+4e-+2H2O===4OH-,故总反应为2Fe+O2+2H2O===2Fe(OH)2,再进一步被氧化为Fe(OH)3,即4Fe(OH)2+O2+2H2O===4Fe(OH)3,Fe(OH)3分解即得铁锈,2Fe(OH)3===Fe2O3·xH2O+(3-x)H2O,故所得铁锈的主要成分为Fe2O3·xH2O,故D正确。
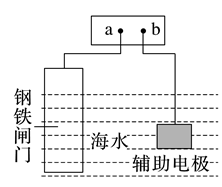
2.钢铁的防护有多种方法,下列对于图中的防护方法描述错误的是( )
资料标签: