






2026届高三考前模拟综合检测(化学)
可能用到的相对分子质量:H-1 O-16 S-32 Cl-35.5
一、单选题(本题共13题,每题3分,共39分。每题只有一个选项最符合题意)
l.第19届杭州亚运会采用石墨烯纳米防滑涂层以增加地面防滑性。石墨烯属于
A. 有机材料 B. 无机非金属材料 C. 金属材料 D. 复合材料
2.印刷电路板的碱性蚀刻液与NaOH溶液共热可发生反应:[Cu(NH3)4]2++2OH– 加热(====)CuO↓+ 4NH3↑+H2O。下列说法不正确的是
A.Cu属于d区元素 B.1 mol [Cu(NH3)4]2+中含16 mol σ键
C.NH3分子所含键角大于H2O D.稳定性:NH3 < H2O
3.一种用于烧制陶瓷的黏土中含Al2Si2O5(OH)4、CaMg(CO3)2、MgSO4等物质。下列说法正确的是
A.离子半径:r(Na+)>r(A13+)>r(O2–) B.电负性:(O)>(C)>(Si)
C.熔点:CaO>MgO D.第一电离能:I1(Si)> I1 (Al)> I1 (Mg)
4.FeS2在酸性条件下可发生反应:FeS2+2H+=Fe2++S+H2S↑。以FeS2为原料制取FeSO4·7H2O
晶体的实验操作或原理不能达到实验目的的是
A.用装置甲制取含FeSO4的悬浊液 B.用装置乙吸收挥发出的H2S气体
C.用装置丙除去S和未反应的FeS2 D.用装置丁蒸干溶液,获得FeSO4·7H2O
阅读下列材料,完成5~7题:
碳族元素及其化合物在自然界广泛存在且具有重要应用。甲烷具有较大燃烧热(890.3 kJ·mol-1),是常见燃料;H2CS3是一种弱酸,在水中缓慢水解生成H2CO3;通过反应Ni(s)+4CO(g)Ni(CO)4(g)可用于提纯Ni。Si、Ge是重要半导体材料,硅可以溶于HF-HNO3的混合酸中生成H2SiF6;醋酸铅(易溶于水,难电离)溶液可以吸收硫化氢气体。
5.下列说法正确的是
A.碳和硅的单质都属于分子晶体
B.CO2中的C原子与SiO2中的Si原子杂化方式相同
C.配合物Ni(CO)4中配位键的形成由Ni提供空轨道
D.Ge原子基态核外电子排布式为[Ar] 4s24p2
6.下列化学反应表示不正确的是
A.甲烷的燃烧:C(g) + 2O2(g)=CO2(g)+ 2O(l) ΔH = -890.3 kJ·mol-1
B.H2CS3与水反应:H2CS3 + 3H2O = H2CO3 + 3H2S
C.硅溶于HF-HNO3的混合酸中:3Si + 4HNO3 + 18HF = 3H2SiF6 + 4NO↑+ 8H2O
D.醋酸铅溶液吸收硫化氢气体:Pb2+ + H2S = PbS↓+ 2H+
7.下列物质结构与性质或性质与用途具有对应关系的是
A.金刚石难溶于水,可用于切割玻璃
B.晶体硅熔点高,可用作半导体材料
C.CH4为正四面体分子,CH4具有较大的燃烧热
D.石墨中碳原子未参与杂化的2p电子可在整个碳原子平面中运动,石墨具有导电性
8.下列物质的转化在给定条件下能实现的是
A.Fe2O3(s)FeCl3(aq)Fe(s)
B.NH3·H2O(aq) (NH4)2SO3(aq)(NH4)2SO4(aq)
C.Ca(ClO)2(aq)HClO(aq)O2(g)
D. CuSO4Cu(OH)2Cu
9. 异甘草素具有抗肿瘤、抗病毒等药物功效。合成中间体Z的部分路线如图:
下列有关化合物X、Y和Z的说法正确的是
A.1molZ中含有6mol碳氧σ键
B.X分子中的所有原子一定共平面
C.Y能发生加成、氧化和消去反应
D.Z与足量的氢气加成后的产物分子中含有3个手性碳原子
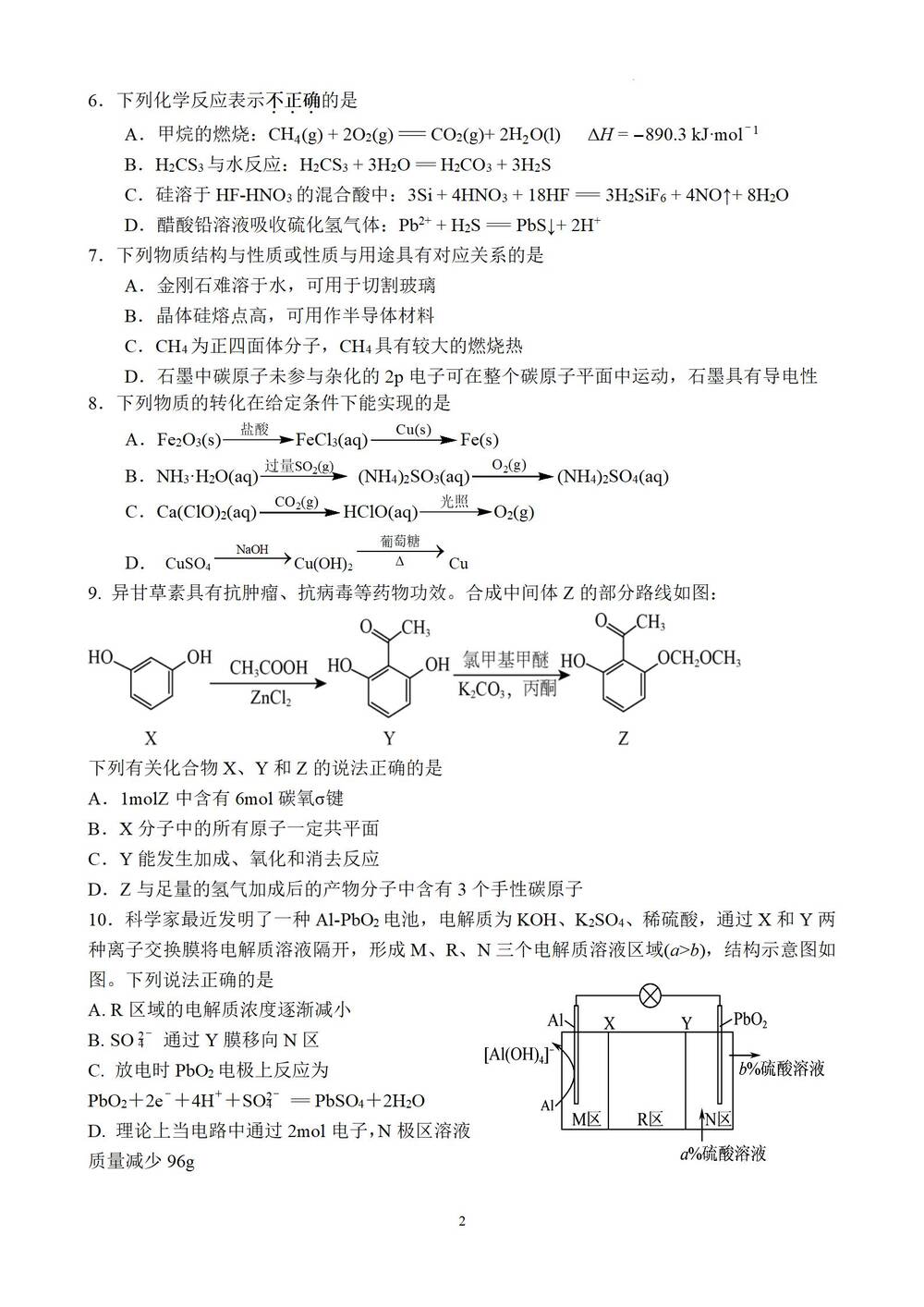
10.科学家最近发明了一种Al-PbO2电池,电解质为KOH、K2SO4、稀硫酸,通过X和Y两种离子交换膜将电解质溶液隔开,形成M、R、N三个电解质溶液区域(a>b),结构示意图如图。下列说法正确的是
A. R区域的电解质浓度逐渐减小
B. SO4(2-)通过Y膜移向N区
C. 放电时PbO2电极上反应为
PbO2+2e-+4H++SO4(2-)== PbSO4+2H2O
D. 理论上当电路中通过2mol电子,N极区溶液质量减少96g