《乙 醛》教学设计
深圳市光明区高级中学 梁国宝
一、课标解读
醛类、酮是《普通高中化学课程标准(2017年版2020年修订)》选择性必修课程主题2“烃及其衍生物的性质与应用”的内容。
1.内容要求
认识醛的组成和结构特点、性质、转化关系及其在生产、生活中的重要应用。
2.学业要求
(1)能写出醛类和酮的官能团、简单代表物(乙醛、甲醛、苯甲醛、丙酮)的结构简式和名称;能够列举简单代表物(乙醛、甲醛、苯甲醛、丙酮)的主要物理性质。
(2)能结合分子结构特点,运用类比迁移的方法分析和推断其他醛的化学性质,并根据有关信息书写相应的化学方程式。
(3)能从官能团和结构变化的角度理解醇、醛、酸的转化关系。能列举甲醛、苯甲醛和丙酮等代表物在生活中的应用,分析和探讨这些物质对人类健康和社会发展可能带来的双重影响。
二、教材分析
本节内容的功能价值(素养功能):能结合醛、酮类物质的官能团及化学键极性特点分析和推断醛、酮类有机物的化学性质,培养学生类比迁移的能力。
人教版新教材在旧教材的基础上增加了醛类、酮两部分的内容。旧教材内容中仅零散的涉及到甲醛的结构、性质和应用,丙酮仅作为拓展知识在“科学视野”中出现。新教材系统的介绍了醛类代表物(甲醛、苯甲醛)、酮(代表物丙酮)。
新教材内容的改变带来的教学启示:教学时不能仅停留于认识乙醛的结构和性质,以及辨识醛与酮的层面,只要求学生掌握醛和酮的化学性质等碎片化知识;而应结合“醇、醛、酸”的转化关系,重视与氧化反应和还原反应等化学知识关联的结构化设计,充分发挥结构化知识对学生核心素养发展的重要作用,同时也为第五节“有机合成”的学习和完成本章最后的“整理与提升”奠定基础。
三、学情分析
学生已有知识、能力等:学生在第二节课已经学习了醇类的典型代表物乙醇的物理性质和化学性质,初步了解了醇、醛、酸之间的相互转化。
但学生的类比迁移能力还有待加强。特殊情况的应变能力不足,如乙醛的银镜反应和新制氢氧化铜反应的探究过程,需要学生反复实验,找到实验关键,能够根据实验现象,推断出反应方程式。对“醇、醛、酸”转化关系模型认识不够深入,应用该模型解决真实问题的能力还需要进一步培养。认识有机物的基本思路和方法(即基于官能团分析、预测、总结归纳物质性质)有待加强。
四、素养目标
【教学目标】
1.从官能团和化学键可能断键部位预测乙醛的化学性质,并能在结构分析和实验事实的基础上书写相关反应的化学方程式,强化“结构决定性质”的观念。
2.通过乙醇、乙醛和乙酸之间的相互转化,加深对有机反应中氧化反应和还原反应的理解,初步构建烃的含氧衍生物间的转化关系。
【评价目标】
1.通过对乙醛性质的预测和探究实验的设计,诊断并发展学生的类比迁移能力和实验探究能力;
2.通过“醇、醛、酸”转化关系模型的建构,并将该模型应用于解决生产和生活中的真实问题,诊断并发展学生对模型的理解和应用能力;
五、教学重点、难点
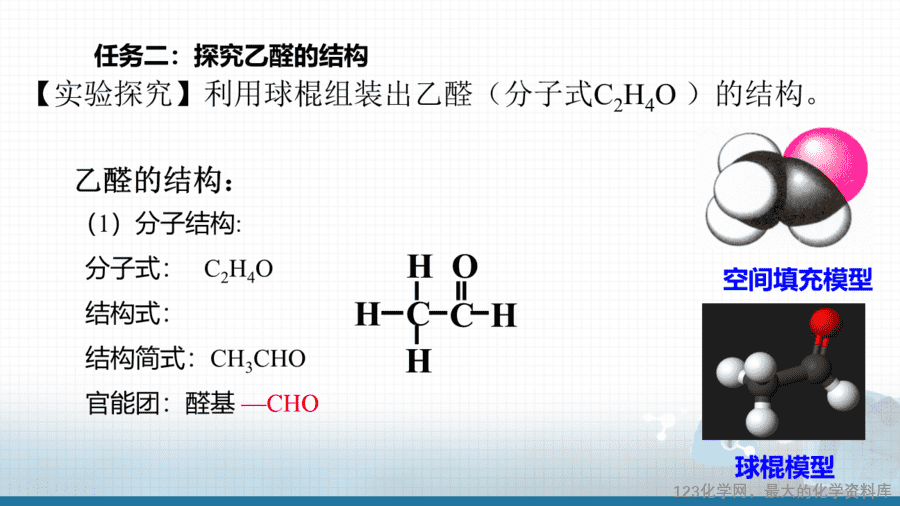
重点:乙醛的结构特点和主要化学性质。
难点:乙醛的氧化反应及相关化学方程式的书写。
六、教学方法
情境导学:创设乙醛生活中的实例真实情境,激发学生学习兴趣。
任务促学:1.探究乙醛的物理性质,加深学生对乙醛的认识
2.乙醛性质的归纳总结,促进学生“醇、醛、酸”转化模型的建立;
3.根据乙醛的结构,预测并探究乙醛的化学性质,进一步加强结构决定性质的理解;
4.探究乙醛的加成反应原理,进一步理解加成反应的实质;
5.乙醛的氧化反应的实验探究,加深对银镜反应和与新制氢氧化铜反应的理解,培养从实验探究,到推断原理的思维模式。
习题测学评价诊学:通过课堂环节中的师生评价、生生评价,以及课堂练习检测等来诊断学生对知识的掌握情况。
实验助学:结合乙醛性质的探究实验,引导学生从“宏观、微观、符号”三重角度学习乙醛的性质。
学案促学:通过学案培养学生提前预习、自主学习的能力。
学 法:交流合作、实验探究、演绎归纳
七、教学思路
本节课先从学生熟悉的生活中的乙醛(喝酒脸红的“罪魁祸首”)引入,结合已学习的乙醇进行深化理解,先预测乙醛的性质,再通过实验探究进行验证。通过具体的化学方程式书写进一步建构“醇、醛、酸”转化关系模型,为后面学习有机合成奠定基础。
通过银镜反应和与新制氢氧化铜反应的实验探究,理解醛基性质在生活中的应用,增强社会责任感。